题目内容
9.能说明非金属性Cl>S的是( )①达到稳定结构时,氯原子只需要1个电子,而硫原子需要2个电子
②氯的含氧酸比硫的含氧酸的酸性强③还原性S2->Cl-
④稳定性HCl>H2S⑤酸性HCl>H2S⑥H2S+Cl2=S↓+2HCl
⑦Cl2与H2在光照或点燃下反应,而硫与H2加热下才反应.
| A. | ②③④⑥ | B. | ③④⑥⑦ | C. | ③④⑤⑥ | D. | 全部 |
分析 元素非金属性强弱的判断依据:最高价氧化物对应水化物的酸性、与氢气化合的难易程度、气态氢化物的稳定性、单质的氧化性,元素非金属性强弱与其原子得电子难易程度有关,据此分析解答.
解答 解:①达到稳定结构时,得电子的难易程度能说明元素非金属性强弱,得电子的数目不能说明元素非金属性强弱,故不选;
②元素对应最高价氧化物的水化物的酸性可以说明元素非金属性强弱,氯的含氧酸比硫的含氧酸的酸性强不能说明元素非金属性强弱,故不选;
③还原性S2->Cl-说明元素非金属性S<Cl,能说明元素非金属性强弱,故选;
④氢化物的稳定性越强说明元素非金属性越强,稳定性HCl>H2S能说明元素非金属性强弱,故选;
⑤元素对应最高价氧化物的水化物的酸性可以说明元素非金属性强弱,酸性HCl>H2S不能说明元素非金属性强弱,故不选;
⑥H2S+Cl2=S↓+2HCl,Cl2能与H2S发生置换反应,说明元素非金属性S<Cl,能说明元素非金属性强弱,故选;
⑦Cl2与H2在光照或点燃下反应,而硫与H2加热下才反应,元素的非金属性越强,其单质的氧化性越强,其单质与氢气化合越容易,Cl2比S容易与H2化合,说明非金属性Cl>S,故选.
故选:B.
点评 本题考查非金属性强弱判断,题目难度不大,侧重考查学生对元素周期律的灵活运用,非金属性强弱与得电子难易程度有关,与得电子多少及物质物理性质无关,为易错题.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
7.关于浓度均为0.1mol•L-1的三种溶液:①氨水 ②盐酸③氯化铵溶液,下列说法错误的是( )
| A. | 溶液的pH:①>③>② | |
| B. | 水电离出的(H+):③>②>① | |
| C. | ①和②等体积混合后的溶液:c(NH4+)+c(H+)=c(Cl-)+c(OH-) | |
| D. | ①和③等体积混合后的溶液呈碱性:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
20.下列反应不属于氧化还原反应的是( )
| A. | CaO+H2O=Ca(OH)2 | B. | 2Na2O2+2H2O=4NaOH+O2↑ | ||
| C. | 2Na+2H2O=2NaOH+H2↑ | D. | 4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
17. 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )| A. | 该反应的化学方程式为6A+2D?3B+4C | |
| B. | 反应进行到1s时,v(A)=v(B) | |
| C. | 反应进行到5s时,v(A)=v(B)=v(C)=v(D) | |
| D. | 反应进行到5s时,B的平均反应速率为0.06mol/(L•s) |
4.下列关于化学反应速率及限度的描述错误的是( )
| A. | 催化剂能改变化学反应的速率 | |
| B. | 一定条件下的可逆反应,反应物不可能100%转化为生成物 | |
| C. | 一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的最大限度 | |
| D. | 当化学反应其最大限度时,反应就停止了 |
14.将0.1mol两种气态烃(其中一种为炔烃)组成的混合气体完全燃烧后得3.36L(标况)CO2和3.6g H2O.则这两种烃的物质的量之比说法正确的是( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 无法计算 |
1.水溶液中能大量共存的一组离子是( )
| A. | K+、Ca2+、OH-、HCO3- | B. | Fe2+、H+、CO32-、Cl- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、SCN- |
18. 现代煤化工产生的H2S是一种重要的工业资源.请回答:
现代煤化工产生的H2S是一种重要的工业资源.请回答:
(1)用过量的NaOH吸收H2S,请写出该反应的离子方程式:H2S+2OH-=S 2-+2H2O.硫化钠又称臭碱,其溶液盛装在带橡胶塞的试剂瓶中,请用离子方程式解释其溶液呈碱性的原因为:S 2-+H2O?HS-+OH-.己知:25℃时,H2S的Ka1=1×10-7,Ka2=1×10-12,计算此温度时1mol/LNa2S溶液的pH=12.(结果取整数)
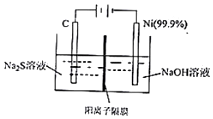
(2)用电解法处理Na2S溶液是处理硫化氢废气的一个重要环节.实验装置如图:
已知阳极的反应为xS2--2(x-1)e-=Sx2-,则阴极的电极反应式是2H++2e-=H2↑或2H2O+2e-=2OH-+H2↑,当反应转移nmole-时,产生标准状况下的气休体积为11.2 n L.
(3)H2S是煤化工原料气脱硫过程的重要中间体.反应原理为:
①COS(g)+H2(g)?H2S(g)+CO(g)△H=+7KJ/mol
②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42KJ/mol
已知断裂1mol气态分子中的化学键所需能量如表所示.
计算表中x=1074.
(4)向2L容积不变的密闭容器中充入2molCOS(g),2molH2(g)和2molH2O(g),进行(3)中所述两个反应,其他条件不变,随着温度升高,CO的平衡体积分数增大,解释其原因为反应①吸热反应,升高温度,平衡正向动,CO的平衡体积分数增大,反应②是放热反应,升温平衡逆向进行,一氧化碳的平衡体积分数也增大.平衡体系中COS的物质的量为1.6mol时,CO的体积分数为5%,则H2O的平衡转化率为5%,反应②的平衡常数为0.30(保留两位有效数字).
 现代煤化工产生的H2S是一种重要的工业资源.请回答:
现代煤化工产生的H2S是一种重要的工业资源.请回答:(1)用过量的NaOH吸收H2S,请写出该反应的离子方程式:H2S+2OH-=S 2-+2H2O.硫化钠又称臭碱,其溶液盛装在带橡胶塞的试剂瓶中,请用离子方程式解释其溶液呈碱性的原因为:S 2-+H2O?HS-+OH-.己知:25℃时,H2S的Ka1=1×10-7,Ka2=1×10-12,计算此温度时1mol/LNa2S溶液的pH=12.(结果取整数)
(2)用电解法处理Na2S溶液是处理硫化氢废气的一个重要环节.实验装置如图:
已知阳极的反应为xS2--2(x-1)e-=Sx2-,则阴极的电极反应式是2H++2e-=H2↑或2H2O+2e-=2OH-+H2↑,当反应转移nmole-时,产生标准状况下的气休体积为11.2 n L.
(3)H2S是煤化工原料气脱硫过程的重要中间体.反应原理为:
①COS(g)+H2(g)?H2S(g)+CO(g)△H=+7KJ/mol
②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42KJ/mol
已知断裂1mol气态分子中的化学键所需能量如表所示.
| 分子 | COS | H2 | H2O | CO | H2S | CO2 |
| 能量/KJ/mol | 1323 | 436 | 926 | X | 678 | 1606 |
(4)向2L容积不变的密闭容器中充入2molCOS(g),2molH2(g)和2molH2O(g),进行(3)中所述两个反应,其他条件不变,随着温度升高,CO的平衡体积分数增大,解释其原因为反应①吸热反应,升高温度,平衡正向动,CO的平衡体积分数增大,反应②是放热反应,升温平衡逆向进行,一氧化碳的平衡体积分数也增大.平衡体系中COS的物质的量为1.6mol时,CO的体积分数为5%,则H2O的平衡转化率为5%,反应②的平衡常数为0.30(保留两位有效数字).
19.用下图所示实验装置进行相应实验,能达到实验目的是( )
| A. | .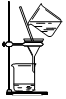 装置可用于除去乙醇中的溴苯 | |
| B. | .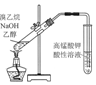 用图所示装置检验溴乙烷与NaOH醇溶液共热产生的C2H4 | |
| C. | .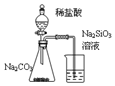 装置可证明非金属性Cl>C>Si | |
| D. |  装置可用于收集O2 |