题目内容
4.下列关于化学反应速率及限度的描述错误的是( )| A. | 催化剂能改变化学反应的速率 | |
| B. | 一定条件下的可逆反应,反应物不可能100%转化为生成物 | |
| C. | 一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的最大限度 | |
| D. | 当化学反应其最大限度时,反应就停止了 |
分析 A.催化剂可改变反应所需的活化能;
B.可逆反应具有可逆性、不完全转化性;
C.平衡状态时为动态平衡,转化率最大;
D.平衡状态时为动态平衡.
解答 解:A.催化剂可改变反应所需的活化能,则能改变化学反应的速率,故A正确;
B.可逆反应具有可逆性、不完全转化性,则反应物不可能100%转化为生成物,故B正确;
C.平衡状态时为动态平衡,可知反应在该条件下所能达到的最大限度,故C正确;
D.平衡状态时为动态平衡,不会停止反应,故D错误;
故选D.
点评 本题考查化学平衡,为高频考点,把握化学平衡的建立、特征为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的易错点,题目难度不大.

练习册系列答案
相关题目
15.下列说法正确的是( )
| A. | 沸点:乙烷>甲烷 | |
| B. | 二氯甲烷有两种不同结构的同分异构体 | |
| C. | 乙二醇和丙三醇为同系物 | |
| D. | 甲苯的一氯代物有三种 |
12.足量的镁与一定量的盐酸反应,减慢反应速度,但又不影响产生H2的量,可以加入的物质是( )
| A. | Al | B. | NaOH | C. | K2CO3 | D. | CH3COONa |
19.下列反应的离子方程式正确的是( )
| A. | 过氧化钠投入水中:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | 烧碱溶液吸收氯气:Cl2+2OH═Cl-+ClO-+H2O | |
| C. | 碳酸钙溶于盐酸:CO32-+2H+═H2O+CO2↑ | |
| D. | 向氯化亚铁溶液中滴入氯水:Fe2++Cl2═Fe3++2Cl- |
9.能说明非金属性Cl>S的是( )
①达到稳定结构时,氯原子只需要1个电子,而硫原子需要2个电子
②氯的含氧酸比硫的含氧酸的酸性强③还原性S2->Cl-
④稳定性HCl>H2S⑤酸性HCl>H2S⑥H2S+Cl2=S↓+2HCl
⑦Cl2与H2在光照或点燃下反应,而硫与H2加热下才反应.
①达到稳定结构时,氯原子只需要1个电子,而硫原子需要2个电子
②氯的含氧酸比硫的含氧酸的酸性强③还原性S2->Cl-
④稳定性HCl>H2S⑤酸性HCl>H2S⑥H2S+Cl2=S↓+2HCl
⑦Cl2与H2在光照或点燃下反应,而硫与H2加热下才反应.
| A. | ②③④⑥ | B. | ③④⑥⑦ | C. | ③④⑤⑥ | D. | 全部 |
16.某烃经催化加氢后,得到2-甲基戊烷,该烃可能的正确名称是( )
| A. | 2-甲基-3-戊炔 | B. | 4-甲基-1,3-戊二烯 | ||
| C. | 2-甲基-2-戊炔 | D. | 2-甲基-3-戊炔 |
13.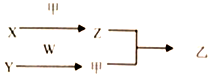 短周期元素A、B、C、D的原子序数依次增加.X、Y、Z、W分別是由这四种元素中的两种组成的常见化合物,甲为单质,乙为红棕色气体,Y为淡黄色固体.上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )
短周期元素A、B、C、D的原子序数依次增加.X、Y、Z、W分別是由这四种元素中的两种组成的常见化合物,甲为单质,乙为红棕色气体,Y为淡黄色固体.上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )
 短周期元素A、B、C、D的原子序数依次增加.X、Y、Z、W分別是由这四种元素中的两种组成的常见化合物,甲为单质,乙为红棕色气体,Y为淡黄色固体.上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )
短周期元素A、B、C、D的原子序数依次增加.X、Y、Z、W分別是由这四种元素中的两种组成的常见化合物,甲为单质,乙为红棕色气体,Y为淡黄色固体.上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )| A. | 原子半径:D>C>B>A | |
| B. | C、D的氢化物均为共价化合物 | |
| C. | 相对分子质量W>X,沸点W>X | |
| D. | B的氢化物常温下一定为气态,C的氢化物常温下为液态 |