题目内容
1.按照要求将相应序号填入空白中:A、O2和O3 B、35Cl和37Cl C、CH3CH2CH3和
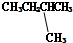 D、H2 和D2
D、H2 和D2E、CH3 CH2CH2OH 和 CH3-O-CH2CH3 F、${\;}_6^{14}C$${\;}_7^{14}N$
(1)B组两种微粒互为同位素;
(2)A组两种物质互为同素异形体;
(3)C组两种物质属于同系物;
(4)E组两物质互为同分异构体;
(5)D组两物质是同一物质.
分析 (1)同一种元素的不同原子间互成同位素;
(2)同一种元素形成的不同单质互成同素异形体;
(3)结构相似,在分子组成上相差一个或若干个CH2的化合物互成同系物;
(4)分子式相同而结构不同的化合物互称同分异构体;
(5)分子式相同而结构也相同的物质为同一种物质.
解答 解:(1)同一种元素的不同原子间互成同位素,故35Cl和37Cl互称同位素,故答案为:B;
(2)同一种元素形成的不同单质互成同素异形体,故O2和O3互称同素异形体,故答案为:A;
(3)结构相似,在分子组成上相差一个或若干个CH2的化合物互成同系物,而CH3CH2CH3和 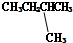 的结构相似,在分子组成上相差一个或若干个CH2的化合物,故互为同系物,故答案为:C;
的结构相似,在分子组成上相差一个或若干个CH2的化合物,故互为同系物,故答案为:C;
(4)分子式相同而结构不同的化合物互称同分异构体,而的CH3CH2CH2OH 和 CH3-O-CH2CH3分子式相同而结构不同的化合物,故互为同分异构体,故答案为:E;
(5)分子式相同而结构也相同的物质为同一种物质,故H2和D2是同一种物质,故答案为:D.
点评 本题考查了”四同”的概念,注意辨析同系物、同分异构体、同位素和同素异形体的概念的区别,难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
3.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | c(I-)=0.1mol•L-1的溶液中:Na+、Mg2+、ClO-、SO42- | |
| B. | 使甲基橙变红色的溶液中:K+、NH4+、HCO3-、Cl- | |
| C. | 与Al反应能放出大量H2的溶液中:Fe2+、Na+、NO3-、Cl- | |
| D. | 由水电离产生的c(OH-)=1×10-10 mol•L-1的溶液中:Ba2+、K+、NO3-、Br- |
12.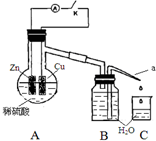 该同学用如下装置进行实验,分析影响反应速率的因素.
该同学用如下装置进行实验,分析影响反应速率的因素.
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示.下列说法不正确的是( )
 该同学用如下装置进行实验,分析影响反应速率的因素.
该同学用如下装置进行实验,分析影响反应速率的因素.| 实验Ⅰ(断开K)1分钟水滴数 | 34 | 59 | 86 | 117 | … | 102 |
| 实验Ⅱ(闭合K)1分钟水滴数 | 58 | 81 | 112 | 139 | … | 78 |
| A. | 实验Ⅰ中化学能主要转化为热能 | |
| B. | 实验Ⅱ中化学能主要转化为电能 | |
| C. | 反应前期水滴数58>34、81>59,主要原因是实验Ⅱ中形成原电池加快反应速率 | |
| D. | 反应后期水滴数102>78,主要原因是实验Ⅰ溶液温度高于实验Ⅱ |
16.对于反应:2SO2+O2?2SO3,下列说法不正确的是( )
| A. | 使用合适的催化剂可以加大反应速率 | |
| B. | 通入过量的O2可以使SO2转化率达到100% | |
| C. | 升高温度可以增大反应速率 | |
| D. | 增大O2浓度可以增大反应速率 |
6.将100mL 0.001mol•L-1的盐酸和50mL pH=3的硫酸溶液混合后,所得溶液的pH为( )
| A. | 4.5 | B. | 2.7 | C. | 3.3 | D. | 3 |
13.下列说法或表示方法中正确的是( )
| A. | 等质量的硫蒸气和硫黄分别完全燃烧,后者放出的热量多 | |
| B. | 氢气的燃烧热为285.5 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol | |
| C. | Ba(OH)2•8H2O(s)+2NH4Cl(s)═=BaCl2(s)+2NH3(g)+10H2O(l)△H<0 | |
| D. | 已知中和热为57.3 kJ/mol,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量要大于57.3 kJ |

 .
. .
.