题目内容
2..某溶液能够使石蕊试液变蓝,则下列离子中一定能大量共存于该溶液的是( )| A. | HCO3-、Ag+、NO3-、Na+ | B. | Na+、Cl-、CO32-、NO3- | ||
| C. | Fe3+、Na+、Cl-、SO42- | D. | H+、Cl-、CO32-、NH4+ |
分析 某溶液能够使石蕊试液变蓝,该溶液呈碱性,溶液中存在大量氢氧根离子,
A.碳酸氢根离子与银离子、氢氧根离子反应,银离子与氢氧根离子反应;
B.四种离子之间不反应,都不与氢氧根离子反应;
C.铁离子与氢氧根离子反应;
D.氢离子、铵根离子与氢氧根离子反应,氢离子与碳酸根离子反应.
解答 解:该溶液能够使石蕊试液变蓝,该溶液呈碱性,溶液中存在大量氢氧根离子,
A.HCO3-、Ag+与氢氧根离子反应,HCO3-、Ag+之间发生双水解反应,在溶液中不能大量共存,故A错误;
B.Na+、Cl-、CO32-、NO3-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.Fe3+与氢氧根离子反应生成氢氧化铁,在溶液中不能大量共存,故C错误;
D.CO32-、H+之间反应,H+、NH4+与氢氧根离子反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 9gD2O和9gH2O中含有的质子数均为5NA | |
| B. | 2L0.5mol/LH2SO3溶液中含有的H+数小于2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
10.下列气体能使品红溶液褪色的是( )
| A. | SO2 | B. | O2 | C. | NH3 | D. | HCl |
14.下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合成稳定化合物的是( )
| A. | 10与12 | B. | 8与17 | C. | 19与17 | D. | 6与14 |
11.下列事实中不能用勒夏特列原理来解释的是( )
| A. | 向H2S水溶液中加入NaOH有利于S2-增多 | |
| B. | 鼓入过量空气有利于SO2转化为SO3 | |
| C. | 高压对合成氨有利 | |
| D. | 500℃左右比室温更有利于合成氨的反应 (合成氨反应是放热反应) |
12.对于化学反应方向的判断,下列说法中正确的是( )
| A. | 温度、压强一定时,放热的熵减小的反应一定能自发进行 | |
| B. | 温度、压强一定时,焓因素和熵因素共同决定一个化学反应的方向 | |
| C. | 反应焓变是决定反应能否进行的惟一因素 | |
| D. | 固体的溶解过程与熵变无关 |
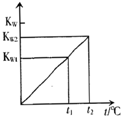 水的离子积常数KW与温度t(℃)的关系如图所示:
水的离子积常数KW与温度t(℃)的关系如图所示: