题目内容
10.下列气体能使品红溶液褪色的是( )| A. | SO2 | B. | O2 | C. | NH3 | D. | HCl |
分析 能使品红溶液褪色说明该物质具有漂白性,依据所给物质的性质解答.
解答 解:氧气、氨气、氯化氢都不具有漂白性,不能使品红溶液褪色,二氧化硫具有漂白性,能够使品红溶液褪色,
故选:A.
点评 本题考查了元素化合物知识,熟悉二氧化硫的漂白性即可解答,题目难度不大.

练习册系列答案
相关题目
20.下列离子方程式正确的是( )
| A. | Na2C2O4水解:C2O42-+2H2O═H2C2O4+2OH- | |
| B. | NH4HSO3溶液与少量NaOH溶液混合:HSO3-+OH-═SO32-+H2O | |
| C. | 将FeS溶液加入过量稀硝酸中:FeS+2H+═Fe2++H2S↑ | |
| D. | 向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═CO32-+2HClO |
1.在100mLNa2CO3与NaAlO2的混合溶液中逐滴加入1mol•L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系,如图所示.下列说法正确的是( )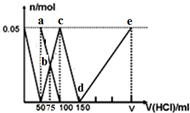

| A. | a点溶液中:c(HCO3-)+c(H2CO3)+c(H+)=c(OH-) | |
| B. | b点所得溶液中阴离子浓度大小顺序为:c(Cl-)>c(HCO3-)>c(CO32-)>c(OH-) | |
| C. | c点溶液中:c(Cl-)+c(HCO3-)+c(H2CO3)+c(CO32-)=1.5 mol•L-1 | |
| D. | d→e的过程中水的电离程度逐渐减小 |
18.常温下,在10mL 0.1mol•L-1 Na2CO3溶液中逐滴加入0.1mol•L-1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法不正确的是( )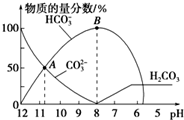

| A. | 在A点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) | |
| B. | 在B点所示的溶液中,浓度最大的离子是Na+ | |
| C. | 当溶液的pH为7时,溶液的总体积大于20mL | |
| D. | 25℃时,CO32-水解常数Kh=2×10-4mol•L-1,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10 |
15.下列实验过程中,不会产生气体的是( )
| A. | 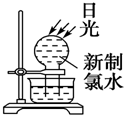 | B. |  | ||
| C. | 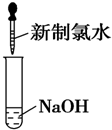 | D. | 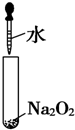 |
2..某溶液能够使石蕊试液变蓝,则下列离子中一定能大量共存于该溶液的是( )
| A. | HCO3-、Ag+、NO3-、Na+ | B. | Na+、Cl-、CO32-、NO3- | ||
| C. | Fe3+、Na+、Cl-、SO42- | D. | H+、Cl-、CO32-、NH4+ |
19.苯丙酸诺龙是一种兴奋剂,结构简式如下,下列有关苯丙酸诺龙的说法中正确的是( )

| A. | 苯丙酸诺龙分子中没有手性碳原子 | |
| B. | 苯丙酸诺龙属于芳香烃 | |
| C. | 苯丙酸诺龙既能使溴的四氯化碳溶液又能使酸性KMnO4溶液褪色 | |
| D. | 1mol苯丙酸诺龙最多可与2 mol的NaOH溶液反应 |
20.下列判断正确的是( )
| A. | 盐酸是化合物 | B. | 只含有一种元素的物质一定是单质 | ||
| C. | CO2、SO2是酸性氧化物 | D. | 纯净物只含有一种元素 |