题目内容
14.下列实验操作能达到实验目的是( )| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将氨水滴加到饱和的FeCl3溶液中并加热 |
| B | 由AlCl3溶液制备无水AlCl3 | 将AlCl3溶液加热蒸干 |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| D | 除去HBr中混有的Br2蒸汽 | 将混合气体通入盛有CCl4的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氯化铁与氨水反应生成氢氧化铁沉淀,无法获得氢氧化铁胶体;
B.加热促进了铝离子的水解,且生成氯化氢易挥发,蒸干后得到的是氢氧化铝沉淀;
C.铜、氧化铜都与稀硝酸反应,违反了除杂原则;
D.HBr不溶于四氯化碳,而溴易溶于四氯化碳,可通过洗气的方法除杂.
解答 解:A.将氨水滴加到饱和的FeCl3溶液中并加热,获得的是氢氧化铁沉淀,无法制备Fe(OH)3胶体,故A错误;
B.由AlCl3溶液制备无水AlCl3,加热时应该在HCl气流中进行,否则最终得到的是氢氧化铝沉淀,故B错误;
C.除去Cu粉中混有的CuO,应该用稀盐酸,否则稀硝酸与Cu和CuO反应,无法达到除杂目的,故C错误;
D.将混合气体通入盛有CCl4的洗气瓶,溴蒸汽易溶于四氯化碳,可除去HBr中混有的Br2蒸汽,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及盐的水解原理、胶体制备、物质分离与提纯等知识,明确常见化学实验基本操作方法即可解答,试题侧重基础知识的考查,有利于提高学生的分析能力及化学实验能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列各图是中学化学常见的几个实验操作,其中错误的是( )
| A. |  | B. |  | C. |  | D. |  |
5.用NA表示阿伏伽德罗常数值,下列说法正确的是( )
| A. | 2.7gAl原子变成离子时,失去电子数为0.1NA | |
| B. | 22.4LCH4 所含的电子数为10NA | |
| C. | 20℃1.01×105Pa时,28gN2所含的原子为NA | |
| D. | 20℃1.01×105Pa时,11.2LO2所含原子数为NA |
9.下列有关原电池的说法中不正确的是( )
| A. | 由 Al、Cu、稀 H2SO4 组成原电池,放电时 SO42-向 Al 电极移动 | |
| B. | 由 Mg、Al、NaOH 溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O | |
| C. | 由 Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出 1 mol Ag时,消耗铜电极32 g | |
| D. | 由 Fe、Cu、FeCl3 溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+ |
19.下列化学用语使用正确的是( )
| A. | HCN分子的结构式:H-C≡N | B. | Se的简化电子排布式:[Ar]4s24p4 | ||
| C. | F-离子的结构示意图: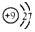 | D. | 二氧化碳的电子式 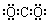 |
6.下列实验中所选用的仪器或实验基本操作合理的是( )
①用10mL量筒准确量取稀硫酸溶液8.0mL;
②为测定熔融氢氧化钠的导电性,将氢氧化钠固体放在石英坩埚中加热熔化
③用干燥的pH试纸测定氯水的pH:
④用过滤的方法除去淀粉胶体中的氯化钠溶液:
⑤用饱和NaHCO3溶液除去CO2中的少量SO2.
①用10mL量筒准确量取稀硫酸溶液8.0mL;
②为测定熔融氢氧化钠的导电性,将氢氧化钠固体放在石英坩埚中加热熔化
③用干燥的pH试纸测定氯水的pH:
④用过滤的方法除去淀粉胶体中的氯化钠溶液:
⑤用饱和NaHCO3溶液除去CO2中的少量SO2.
| A. | ①③ | B. | ②③④ | C. | ①③⑤ | D. | ①⑤ |
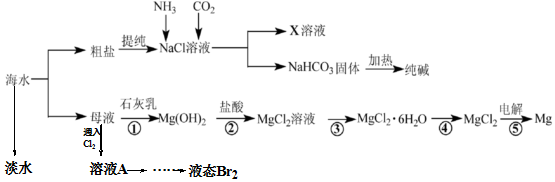
4.水资源非常重要,下列说法错误的是( )
| A. | 蒸馏法是海水谈化的方法之一 | |
| B. | 海水中的${\;}_{92}^{235}$U元素经浓缩提炼后可作核反应堆燃料 | |
| C. | 海水中的Li元素属于微量元素,提炼后可作Li电池原料 | |
| D. | 0℃以上,温度越高,水的密度越小 |