题目内容
5.用NA表示阿伏伽德罗常数值,下列说法正确的是( )| A. | 2.7gAl原子变成离子时,失去电子数为0.1NA | |
| B. | 22.4LCH4 所含的电子数为10NA | |
| C. | 20℃1.01×105Pa时,28gN2所含的原子为NA | |
| D. | 20℃1.01×105Pa时,11.2LO2所含原子数为NA |
分析 A、求出铝的物质的量,然后根据铝反应后变为+3价;
B、甲烷所处的状态不明确;
C、求出氮气的物质的量,然后根据氮气为双原子分子来分析;
D、20℃1.01×105Pa时,气体摩尔体积大于22.4L/mol.
解答 解:A、2.7g铝的物质的量为0.1mol,而铝反应后变为+3价,故0.1mol铝失去0.3NA个电子,故A错误;
B、甲烷所处的状态不明确,故甲烷的物质的量和含有的电子个数无法计算,故B错误;
C、28g氮气的物质的量为1mol,而氮气为双原子分子,故1mol氮气中含2NA个,故C正确;
D、20℃1.01×105Pa时,气体摩尔体积大于22.4L/mol,故11.2L氧气的物质的量小于0.5mol,则含有的原子个数小于NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
2.某酯Q的分子式为C4H8O2,下列醇和羧酸在浓硫酸作催化剂的条件下发生酯化反应能生成Q的是( )
| A. | 甲酸(HCOOH)与正丁醇 | B. | 乙酸与甲醇(CH3OH) | ||
| C. | 乙醇与CH3CH2COOH | D. | CH3CH2COOH与甲醇(CH3OH) |
20.化学 与生产、生活息息相关,下列叙述错误的是( )
| A. | 光催化还原水制氢比电解水制氢更节能环保、更经济 | |
| B. | 铁表面镀锌可增强其抗腐蚀性 | |
| C. | 用聚乙烯塑料代替聚乳酸塑料可减少白色污染 | |
| D. | 制饭勺、饭盒、高压锅等的不锈钢是合金 |
17.分子式为C6H10O4,且能与NaHCO3反应的只含一种官能团的有机物共有(不含立体异构)( )
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
14.下列实验操作能达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将氨水滴加到饱和的FeCl3溶液中并加热 |
| B | 由AlCl3溶液制备无水AlCl3 | 将AlCl3溶液加热蒸干 |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| D | 除去HBr中混有的Br2蒸汽 | 将混合气体通入盛有CCl4的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
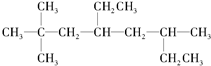 烃A的一氯代物具有不同沸点的产物有10种.
烃A的一氯代物具有不同沸点的产物有10种.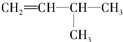 的系统名称是3-甲基-1-丁烯,将其在催化剂存在下完全氢化,所得烷烃的系统名称是2-甲基丁烷.
的系统名称是3-甲基-1-丁烯,将其在催化剂存在下完全氢化,所得烷烃的系统名称是2-甲基丁烷.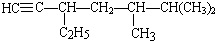 的系统名称是5,6-二甲基-3-乙基-1-庚烯,将其在催化剂存在条件下完全氢化,所得烷烃的系统名称为2,3-二甲基-5-乙基-庚烷.
的系统名称是5,6-二甲基-3-乙基-1-庚烯,将其在催化剂存在条件下完全氢化,所得烷烃的系统名称为2,3-二甲基-5-乙基-庚烷. .
.