题目内容
15.关于反应CH3COOH+CH3CH2OH?CH3COOCH2CH3+H2O,下列说法错误的是( )| A. | 该反应是可逆反应 | |
| B. | 升高温度可以加快反应速率 | |
| C. | 使用催化剂可以加快反应速率 | |
| D. | 使用过量乙醇能使乙酸完全转化为乙酸乙酯 |
分析 为可逆反应,反应物不可能完全转化为生成物,一般来说,增大浓度、升高温度或加入催化剂,则增大反应速率,以此解答该题.
解答 解:A.由方程式可知该反应为可逆反应,故A正确;
B.升高温度,增大活化分子的百分数,反应速率增大,故B正确;
C.加入催化剂,可增大活化分子的百分数,增大反应速率,故C正确;
D.为可逆反应,反应物不可能完全转化,故D错误.
故选D.
点评 本题易酯化反应为载体考查化学反应素的影响因素,为高频考点,侧重于学生的分析能力和基本概念、理论知识的综合理解和运用的考查,难度不大,注意把握可逆反应的特点.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
5.已知A、B、D、E 均为中学化学常见物质,它们之间的转化关系如图所示(部分产物略去,①②③④的反应条件相同).则A、E 可能的组合为( )
①CO2、NaOH 溶液 ②NaCl溶液、Ca(OH)2 溶液③Fe、稀HNO3 ④Na、O2 ⑤CuO、C ⑥AlCl3 溶液、NH3•H2O.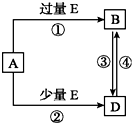
①CO2、NaOH 溶液 ②NaCl溶液、Ca(OH)2 溶液③Fe、稀HNO3 ④Na、O2 ⑤CuO、C ⑥AlCl3 溶液、NH3•H2O.

| A. | ②③④⑤ | B. | ①③④⑤⑥ | C. | ①②③⑤⑥ | D. | ①③⑤ |
6.下列有关物质的性质或用途的叙述中,正确的是( )
| A. | 常温下,运输浓硫酸、浓硝酸时可用铝制或铁制槽车 | |
| B. | 用氯化钡溶液可区别SO42-和CO32-离子 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 二氧化硅是一种酸性氧化物,它不跟任何酸发生反应 |
3.纸是传承人类文明的载体之一.纸的主要化学成分是( )
| A. | 纤维素 | B. | 蛋白质 | C. | 塑料 | D. | 淀粉 |
10.在含有较多NH4+、Ba2+、Cl-的溶液中还能大量共存的离子是( )
| A. | SO42- | B. | OH- | C. | Ag+ | D. | Mg2+ |
20.某溶液中可能含有下列5种离子中的某几种:Na+、NH4+、Fe3+、Al3+、Clˉ.为确认该溶液组成进行如下实验:
①取20.0mL该溶液,加入20.0mL 4.00mol•L-1NaOH溶液,生成红褐色沉淀且没有刺激性气体生成.将沉淀过滤、洗涤、灼烧,得固体0.80g.再将滤液稀释至100mL,测得滤液中c(OHˉ)为0.10mol•L-1;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀8.61g.
由此可得出原溶液组成的正确结论是( )
①取20.0mL该溶液,加入20.0mL 4.00mol•L-1NaOH溶液,生成红褐色沉淀且没有刺激性气体生成.将沉淀过滤、洗涤、灼烧,得固体0.80g.再将滤液稀释至100mL,测得滤液中c(OHˉ)为0.10mol•L-1;
②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀8.61g.
由此可得出原溶液组成的正确结论是( )
| A. | 一定含有Fe3+、Al3+、Clˉ,不含Na+、NH4+ | |
| B. | 一定含有Na+、Fe3+、Clˉ,不含NH4+,可能含有Al3+ | |
| C. | c (Al3+)=1.00 mol•L-1 | |
| D. | c(Na+)=0.50 mol•L-1 |
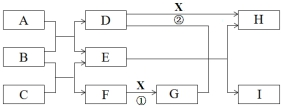
 .
.