题目内容
4.已知3X(g)+2Y(g)?nZ(g)+2W(g),若将0.6mol X和0.4mol Y混合充入一密闭体积可调的容器中,压强保持不变,5min后体积变为原来的1.2倍,则n值是( )| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
分析 压强不变时,气体的物质的量与容器容积成正比;向压强不变的容器中充入0.6mol X和0.4mol Y后,容器容积变为原来的1.2倍,说明反应后气体体积增大,则3+2<n+2,据此判断n的范围.
解答 解:若将0.6mol X和0.4mol Y混合充入一密闭体积可调的容器中,压强保持不变,5min后体积变为原来的1.2倍,说明反应后气体物质的量增大,
则可逆反应3X(g)+2Y(g)?nZ(g)+2W(g)的正反应是气体体积增大的反应,即:3+2<n+2,解得:n>3,
选项中只有D符合,
故选D.
点评 本题考查了化学平衡的计算,题目难度不大,明确容器压强不变时气体的物质的量与容器容积成正比为解答关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
14.有些古文或谚语包含了丰富的化学知识,从化学角度解释下列古文或谚语,其中不正确的是( )
| 选项 | 古文或谚语 | 化学解释 |
| A | 日照香炉生紫烟 | 碘的升华 |
| B | 以曾青涂铁,铁赤色如铜 | 置换反应 |
| C | 煮豆燃豆箕,豆在斧中泣 | 化学能转化为热能 |
| D | 雷雨肥庄稼 | 自然界固氮作用 |
| A. | A | B. | B | C. | C | D. | D |
15.关于反应CH3COOH+CH3CH2OH?CH3COOCH2CH3+H2O,下列说法错误的是( )
| A. | 该反应是可逆反应 | |
| B. | 升高温度可以加快反应速率 | |
| C. | 使用催化剂可以加快反应速率 | |
| D. | 使用过量乙醇能使乙酸完全转化为乙酸乙酯 |
12.下列叙述正确的是( )
| A. | 等质量的乙烯与乙醇充分燃烧时消耗氧气的质量相等 | |
| B. | 生活中用于制造水杯、奶瓶、食物保鲜膜等用品的聚氯乙烯是通过加聚反应得到的 | |
| C. | 分子式为C6H12的某链状有机物,6个碳原子肯定在同一平面上,则与氢气加成后产物的名称为2,3-二甲基丁烷 | |
| D. | 红斑素、红曲素是常用于糖果、雪糕等食品的着色剂的主要成分,结构分别如图所示: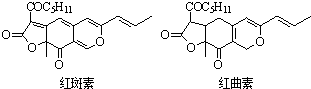 太阳能光触媒则红斑素和红曲素互为同分异构体 |
19.常温下(25℃),已知H2SO3电离常数Ka1=1.4×10-2,Ka2=6.3×10-4,NH3•H2O的常数Kb=1.8×10-3.则下列有关NH4HSO3溶液的叙述正确的是( )
| A. | 该溶液中,Na+、Cl-、S2-和SO42-可以大量共存 | |
| B. | 含等物质的量的NH4HSO3与NaOH溶液混合,反应的离子方程式为:HSO3-+OH-=SO32-+H2O | |
| C. | NH4HSO3为弱酸弱碱盐,其水溶液pH>7 | |
| D. | c(NH4+)>c(HSO3-)>c(SO32-)>C(H2SO3)>C(NH3•H2O) |
9.下列关于实验原理或操作的叙述不正确的是( )
| A. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| B. | 利用重结晶可对粗苯甲酸进行提纯 | |
| C. | 不能用核磁共振氢谱来鉴别1-溴丙烷和2-溴丙烷 | |
| D. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 |
4.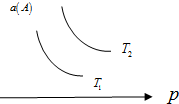 在一定条件下,某可逆反应aA(g)+bB(s)?cC(g)达到平衡后,A的转化率a(A)与温度(T)、压强(p)的关系如图所示,根据图象,下列判断正确的是( )
在一定条件下,某可逆反应aA(g)+bB(s)?cC(g)达到平衡后,A的转化率a(A)与温度(T)、压强(p)的关系如图所示,根据图象,下列判断正确的是( )
 在一定条件下,某可逆反应aA(g)+bB(s)?cC(g)达到平衡后,A的转化率a(A)与温度(T)、压强(p)的关系如图所示,根据图象,下列判断正确的是( )
在一定条件下,某可逆反应aA(g)+bB(s)?cC(g)达到平衡后,A的转化率a(A)与温度(T)、压强(p)的关系如图所示,根据图象,下列判断正确的是( )| A. | a+b<c | |
| B. | 若T2>T1,则该反应在高温下易自发进行 | |
| C. | △H>0 | |
| D. | 若T2<T1,则该反应一定不能自发进行 |
2. Al、Ti、Fe、Cu是几种常见的重要金属.根据要求回答下列问题:
Al、Ti、Fe、Cu是几种常见的重要金属.根据要求回答下列问题:
(1)在火箭和导弹技术中,将铝粉与石墨、TiO2按一定比例混合均匀,涂在金属表面,在高温下煅烧,金属表面生成TiC和另外一种耐高温物质X,写出该反应的化学方程式4Al+3C+3TiO2$\frac{\underline{\;高温\;}}{\;}$3TiC+2Al2O3.
(2)Fe原子的价电子排布式为3d64s2,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.Fe和Mn的部分电离能数据如右表:
其中表示Fe电离能数据的是B (填A或B).
(3)向CuSO4溶液中加入氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液;最后向溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4•H2O(注:[Cu(NH3)4]2+为平面正四边形结构),该晶体存在的粒子中空间构型为正四面体的是SO42-,与其互为等电子体的分子为SiF4、CCl4(GeCl4)(写出两个即可);N原子的杂化方式为sp3.
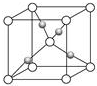
(4)Cu2O的晶胞结构如图所示,Cu+的配位数为2,该晶胞的边长为a pm,则Cu2O的密度为$\frac{288×1{0}^{30}}{{a}^{3}×{N}_{A}}$g/cm3(阿佛加德罗常数用NA表示,1m=1012pm)
 Al、Ti、Fe、Cu是几种常见的重要金属.根据要求回答下列问题:
Al、Ti、Fe、Cu是几种常见的重要金属.根据要求回答下列问题:(1)在火箭和导弹技术中,将铝粉与石墨、TiO2按一定比例混合均匀,涂在金属表面,在高温下煅烧,金属表面生成TiC和另外一种耐高温物质X,写出该反应的化学方程式4Al+3C+3TiO2$\frac{\underline{\;高温\;}}{\;}$3TiC+2Al2O3.
(2)Fe原子的价电子排布式为3d64s2,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.Fe和Mn的部分电离能数据如右表:
| 元素 | A | B | |
| 电离能(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(3)向CuSO4溶液中加入氨水生成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液;最后向溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4•H2O(注:[Cu(NH3)4]2+为平面正四边形结构),该晶体存在的粒子中空间构型为正四面体的是SO42-,与其互为等电子体的分子为SiF4、CCl4(GeCl4)(写出两个即可);N原子的杂化方式为sp3.
(4)Cu2O的晶胞结构如图所示,Cu+的配位数为2,该晶胞的边长为a pm,则Cu2O的密度为$\frac{288×1{0}^{30}}{{a}^{3}×{N}_{A}}$g/cm3(阿佛加德罗常数用NA表示,1m=1012pm)