题目内容
1.相同条件下,同质量的X、Y两种气体,相对分子质量分别为A、B,则它们的体积比为B:A,分子个数比为B:A,密度比为A:B.分析 根据n=$\frac{m}{M}$可知,相同质量的气体物质的量之比与摩尔质量成反比,再根据V=nVm可知,相同条件下气体体积之比等于物质的量之比;分子个数比为物质的量之比;根据相同条件下,密度之比等于摩尔质量之比.
解答 解:X、Y两种气体分子的相对分子质量分别为A、B.
同温同压下,根据n=$\frac{m}{M}$可知,同质量的X、Y气体物质的量之比=Bg/mol:Ag/mol=B:A,再根据V=nVm可知,相同条件下气体体积之比等于物质的量之比=B:A,分子个数比为物质的量之比=B:A;根据相同条件下,密度之比等于摩尔质量之比=Ag/mol:Bgmol=A:B,故答案为:B:A;B:A;A:B.
点评 本题考查物质的量的有关计算等,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
11.钢铁腐蚀发生得最普遍的是( )
| A. | 化学腐蚀 | B. | 析氢腐蚀 | C. | 吸氧腐蚀 | D. | 钝化 |
12.下列除杂试剂(括号内为杂质)选择正确的是( )
| A. | CO2(SO2):澄清石灰水 | B. | CO2(CO):通入氧气,并加热 | ||
| C. | Cl2(HCl):饱和碳酸钠溶液 | D. | Fe(Al):烧碱溶液 |
9.下列各物质的中心原子采用sp3杂化的是( )
| A. | NH3 | B. | O3 | C. | CO2 | D. | BeCl2 |
16.下列实验装置正确且能达到实验目的是( )

| A. | 甲装置:测定盐酸的物质的量浓度 | |
| B. | 乙装置:验证H2SO4、H2CO3、H2SiO3酸性的强弱 | |
| C. | 丙装置:实验室制备乙酸乙酯 | |
| D. | 丁装置:比较碳酸钠和碳酸氢钠的热稳定性 |
6.某工厂的电镀污泥中含有铜、铁等金属化合物.为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

(1)酸浸后加入H2O2的目的是将Fe2+氧化成Fe3+,便于调整pH值与Cu2+分离.调pH步骤中加入的试剂最好是CuO、或Cu(OH)2、或CuCO3(填化学式).实验室进行过滤操作所用到的玻璃仪器有漏斗、烧杯、玻璃棒.
(2)向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式2CuSO4+2NaCl+Na2SO3+H2O=2CuCl↓+2Na2SO4+H2SO4.
(3)CuCl产品中CuCl的质量分数大于96.50%为国家合格标准.称取所制备的CuCl样品0.2500g置于一定量的0.5mol/LFeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol/L的Ce(SO4)2溶液滴定,到达滴定终点时消耗Ce(SO4)2溶液24.60mL.有关的化学反应为:Fe3++CuCl═Fe2++Cu2++Cl-,Ce4++Fe2+═Fe3++Ce3+,通过计算说明该CuCl样品符合(填“符合”或“不符合”)国家标准.
(4)25℃时,Ksp[Fe(OH]3]=4.0×10-38.Fe3+发生水解反应Fe3++3H2O?Fe(OH)3+3H+,该反应的平衡常数为2.5×10-5.

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.3 | 7.6 | 4.4 |
| 完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(2)向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式2CuSO4+2NaCl+Na2SO3+H2O=2CuCl↓+2Na2SO4+H2SO4.
(3)CuCl产品中CuCl的质量分数大于96.50%为国家合格标准.称取所制备的CuCl样品0.2500g置于一定量的0.5mol/LFeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol/L的Ce(SO4)2溶液滴定,到达滴定终点时消耗Ce(SO4)2溶液24.60mL.有关的化学反应为:Fe3++CuCl═Fe2++Cu2++Cl-,Ce4++Fe2+═Fe3++Ce3+,通过计算说明该CuCl样品符合(填“符合”或“不符合”)国家标准.
(4)25℃时,Ksp[Fe(OH]3]=4.0×10-38.Fe3+发生水解反应Fe3++3H2O?Fe(OH)3+3H+,该反应的平衡常数为2.5×10-5.
13. 对实验Ⅰ~Ⅳ的实验操作现象判断正确的是( )
对实验Ⅰ~Ⅳ的实验操作现象判断正确的是( )
 对实验Ⅰ~Ⅳ的实验操作现象判断正确的是( )
对实验Ⅰ~Ⅳ的实验操作现象判断正确的是( )| A. | 实验Ⅰ:产生红褐色沉淀 | B. | 实验Ⅱ:溶液颜色变红 | ||
| C. | 实验Ⅲ:放出大量气体 | D. | 实验Ⅳ:先出现白色沉淀,后溶解 |
10.25℃时,等体积等浓度的NaHCO3和Na2CO3溶液中,下列判断错误的是( )
| A. | 均存在电离平衡 | B. | 阴离子数目前者大于后者 | ||
| C. | c(OH-)前者小于后者 | D. | 存在的粒子种类相同 |
 .
. 名称是2,4二甲基-4-乙基庚烷.
名称是2,4二甲基-4-乙基庚烷. )的官能团的名称为碳碳双键、羟基.
)的官能团的名称为碳碳双键、羟基. .
. 形成六元环酯的反应
形成六元环酯的反应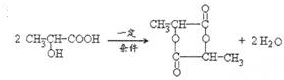 .
.