��Ŀ����
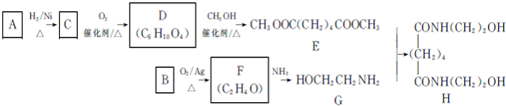
8������A�ͷ�����DΪԭ�Ϻϳɻ�����X��·����ͼ��ʾ��
��֪���ٷ�ӦA��BΪ�ӳɷ�Ӧ��
��RCHO+CH3COOR��$\stackrel{CH_{3}CH_{2}ONa}{��}$RCH=CHCOOR�䣮
�ش��������⣺
��1��A�к��й����ŵ�������̼̼�μ���F�������DZ��״���
��2��E����F�ķ�Ӧ������ȡ����Ӧ��
��3����ӦC+F���Ļ�ѧ����ʽΪ
 ��
����4����ӦF��H�Ļ�ѧ����ʽΪ
 ��
����5��X�Ľṹ��ʽΪ
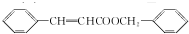 �����й���X��˵������ȷ����bc������ĸ����
�����й���X��˵������ȷ����bc������ĸ����a���ܷ���ˮ�ⷴӦ b���ܷ���������Ӧ
c������ʹBr2��CCl4��Һ��ɫ d������Ũ���ᷢ��ȡ����Ӧ
��6�������廯����M��G��ͬ���칹�壬M����NaHCO3��Һ��Ӧ�������壬����������M��14�֣����к˴Ź���������4����ҷ����֮��Ϊ6��2��1��1����
 ��
�� ����ṹ��ʽ����
����ṹ��ʽ����
���� ��A��B��ӦΪ�ӳɷ�Ӧ������B�ķ���ʽ��֪��AΪHC��CH��BΪCH3CHO��B����������Ӧ���� CΪCH3COOH������E��H�ķ���ʽ��Eת����F��Fת����H������ ��֪��EΪ ��E��������ˮ���FΪ
��E��������ˮ���FΪ ��F����������Ӧ����HΪ
��F����������Ӧ����HΪ �����Է�����DΪ�ױ���C��F��Ũ���������·���������Ӧ����GΪ
�����Է�����DΪ�ױ���C��F��Ũ���������·���������Ӧ����GΪ ��G��H������Ϣ���еķ�Ӧ����XΪ
��G��H������Ϣ���еķ�Ӧ����XΪ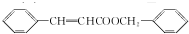 ���ݴ˴��⣻
���ݴ˴��⣻
��� �⣺��A��B��ӦΪ�ӳɷ�Ӧ������B�ķ���ʽ��֪��AΪHC��CH��BΪCH3CHO��B����������Ӧ���� CΪCH3COOH������E��H�ķ���ʽ��Eת����F��Fת����H������ ��֪��EΪ ��E��������ˮ���FΪ
��E��������ˮ���FΪ ��F����������Ӧ����HΪ
��F����������Ӧ����HΪ �����Է�����DΪ�ױ���C��F��Ũ���������·���������Ӧ����GΪ
�����Է�����DΪ�ױ���C��F��Ũ���������·���������Ӧ����GΪ ��G��H������Ϣ���еķ�Ӧ����XΪ
��G��H������Ϣ���еķ�Ӧ����XΪ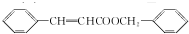 ��
��
��1��AΪHC��CH��A�к��й����ŵ�������̼̼�μ���FΪ ��F�������DZ��״���
��F�������DZ��״���
�ʴ�Ϊ��̼̼�μ������״���
��2����������ķ�����֪��E����F�ķ�Ӧ������ ȡ����Ӧ��
�ʴ�Ϊ��ȡ����Ӧ��
��3��CΪCH3COOH��FΪ ����ӦC+F���Ļ�ѧ����ʽΪ
����ӦC+F���Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��4��F����������Ӧ����H����ӦF��H�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��5����������ķ�����֪��X�Ľṹ��ʽΪ 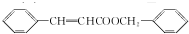 ��
��
a��X�����������ܷ���ˮ�ⷴӦ������ȷ��
b��X��û��ȩ�������Բ��ܷ���������Ӧ���ʴ���
c��X��̼̼˫������ʹBr2��CCl4��Һ��ɫ���ʴ���
d��X���б���������Ũ���ᷢ��ȡ����Ӧ������ȷ����ѡbc��
�ʴ�Ϊ��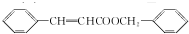 ��bc��
��bc��
��6��GΪ �������廯����M��G��ͬ���칹�壬M����NaHCO3��Һ��Ӧ�������壬˵�����Ȼ�������������MΪ����������һ������Ϊ-CH2CH2COOH��-CH��CH3��COOH��Ҳ�����������������ţ�Ϊ-CH3��-CH2COOH����Ϊ-CH2CH3��-COOH��ÿ�ֶ����ڼ�����֣�Ҳ���������ֻ��ţ�Ϊ-CH3��-CH3��-COOH�����ݶ�����һ��ԭ����6�֣����Թ���1+1+3+3+6=14 �֣����к˴Ź���������4����ҷ����֮��Ϊ6��2��1��1����
�������廯����M��G��ͬ���칹�壬M����NaHCO3��Һ��Ӧ�������壬˵�����Ȼ�������������MΪ����������һ������Ϊ-CH2CH2COOH��-CH��CH3��COOH��Ҳ�����������������ţ�Ϊ-CH3��-CH2COOH����Ϊ-CH2CH3��-COOH��ÿ�ֶ����ڼ�����֣�Ҳ���������ֻ��ţ�Ϊ-CH3��-CH3��-COOH�����ݶ�����һ��ԭ����6�֣����Թ���1+1+3+3+6=14 �֣����к˴Ź���������4����ҷ����֮��Ϊ6��2��1��1���� ��
�� ��
��
�ʴ�Ϊ��14�� ��
�� ��
��
���� ���⿼���л�����ƶ���ϳɡ������Žṹ�����ʡ���������ͬ���칹����д�ȣ�ע�������л�������ŵ����ʺ�ת������Ϸ�Ӧ�������л���ṹ���з������Ѷ��еȣ�

| ѡ�� | ʵ����� | ʵ��Ŀ�� |
| A | ���ȵ�NaOH��Һ�е��뱥��FeCl3��Һ | �Ʊ�Fe��OH��3���� |
| B | ��SO2ͨ��KMnO4��Һ | ��֤SO2��Ư���� |
| C | ������Fe3+��MgCl2��Һ�м�������MgCO3��ĩ�����ȡ����貢���� | ��ȥMgCl2��Һ��������Fe3+ |
| D | ��0.1mol•L-1��Na2SO4��Һ����BaCl2��Һ�������г����������ٵμ�0.1mol•L-1��Na2CO3��Һ | �Ƚ�BaCO3��BaSO4�ܶȻ��Ĵ�С |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ��AԪ�صĵ縺�Դ��ϵ�����������AԪ�صĵ縺�Դ��ϵ�����С | |
| B�� | �縺�ԵĴ�С������Ϊ����Ԫ�صĽ����Ժͷǽ�����ǿ���ij߶� | |
| C�� | ��ԭ����ֻ��һ�����ӣ�����ԭ��ֻ��һ��ԭ�ӹ�� | |
| D�� | NaH�Ĵ�����֧�ֿɽ���Ԫ�ط��ڢ�A�Ĺ۵� |
| A�� | ����ʧȥ�ĵ���������� | |
| B�� | ��������С�ĵ���������� | |
| C�� | 2p���������������2s����������� | |
| D�� | ���������������˶��ĵ���������� |
| ���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� |
��2��������������ˮ�����У�������ǿ�Ļ�����ķ���ʽ��HClO4��������ǿ�Ļ�����ĵ���ʽ�ǣ�
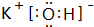 ��
����3��д��Ԫ�آٶ�Ӧ�����������ĽṹʽΪO=C=O��������ľ����к��е��������� �������Ӽ��ۼ�����Ӽ������������ۼ������Ӽ�������
��4���٢ڢۢ�������Ԫ�ض�Ӧ�ļ��⻯��е���ߵ���H2O��NH3��H2S��CH4
��5���ۢܢݢ�������Ԫ�ض�Ӧ�����Ӱ뾶�ɴ�С��˳��S2-��O2-��Na+��Al3+��

 ��
��
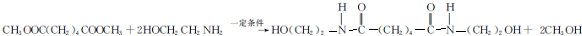 ��
��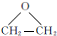 ���ܷ���������Ӧ��F��ͬ���칹����CH3CHO��
���ܷ���������Ӧ��F��ͬ���칹����CH3CHO��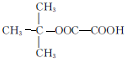 ��д�ṹ��ʽ����
��д�ṹ��ʽ����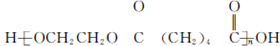 �ĺϳ�·�ߣ�
�ĺϳ�·�ߣ�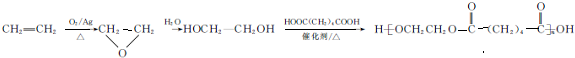 ��
�� ������Ϊ2��3-����-2-��ϩ��A�е�̼ԭ���Ƿ���ͬһƽ�棿�ǣ���ǡ����ǡ�����
������Ϊ2��3-����-2-��ϩ��A�е�̼ԭ���Ƿ���ͬһƽ�棿�ǣ���ǡ����ǡ�����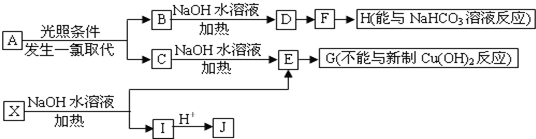
 ��
�� ��
�� ����������A��д�ṹ��ʽ��
����������A��д�ṹ��ʽ�� ����Ӧ������������Ӧ��
����Ӧ������������Ӧ�� +2NaOH$\stackrel{��}{��}$
+2NaOH$\stackrel{��}{��}$ +
+ +H2O
+H2O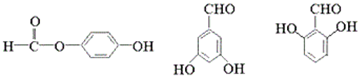 ����һ�֣�
����һ�֣�