��Ŀ����
15��Na2O2������Ư���ͺ�������еĹ���������1��ijѧϰС�鷢�֣���ʢ��Na2O2���Թ��м�������ˮ��������ȫ�ܽ⣬�����������������ݣ���������ʧ�������е���1��2�η�̪��Һ����Һ��죻���Թ���������ɫ�ܿ���ȥ����ʱ�����Թ��м�������MnO2��ĩ���������ݲ�����
��ʹ��̪��Һ�������Ϊ�������ƺ�ˮ��Ӧ���ɼ��������ƣ���ɫ��ȥ�Ŀ���ԭ���Ƿ�Ӧ���ɵ�H2O2����Ư�����ã�
�ڼ���MnO2��Ӧ�Ļ�ѧ����ʽΪ2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����
��2��Na2O2��ǿ�����ԣ�H2���л�ԭ�ԣ���ͬѧ����Na2O2��H2�ܷ�Ӧ��Ϊ����֤�˲��룬��С��ͬѧ��������ʵ�飬ʵ�鲽����������£�

����1������ͼ��װ������ͼ�мг�����ʡ�ԣ�����������ԣ�װ��ҩƷ��
����2����K1��K2����������������װ��Na2O2��Ӳ�ʲ����ܣ�һ��ʱ���û���κ�����
����3������H2�Ĵ��Ⱥ�ʼ���ȣ��۲쵽Ӳ�ʲ�������Na2O2��ʼ�ۻ�������ɫ�ķ�ĩ����˰�ɫ���壬�����������ͭδ����ɫ��
����4����Ӧ��ȥ�ƾ��ƣ���Ӳ�ʲ�������ȴ��ر�K1��
������ϡ��������������dz���©����Bװ�õ����������������е��������壮
�ڱ�������������ȵ�ԭ���Ƿ�ֹ������������ϼ��ȱ�ը��
������װ��D��Ŀ���Ƿ�ֹ�����еĶ�����̼��ˮ��������Cװ�ú������Ʒ�ӦӰ��ʵ����֤��
����õ��Ľ����������������Ʒ�Ӧ�����������ƣ�Na2O2+H2$\frac{\underline{\;\;��\;\;}}{\;}$2NaOH�����ܷ�Ӧ���û�ѧ����ʽ��ʾ����
���� ��1���ٹ������ƺ�ˮ��Ӧ�������������Ǽ������̪��죻��ɫ��ȥ�Ŀ���ԭ���ǹ������ƺ�ˮ��Ӧ���ɵĹ���������������ԣ�
�ڹ��������ڶ��������������ֽ�����ˮ��������
��2���ٷ���װ��ͼ��ʵ�鲽���֪��ʢ���������Ϊ����©����Bװ���dz�ȥ�����е�ˮ������
�������ǿ�ȼ��������п����ҵ�ȼ������ը��
��Dװ���Ƿ�ֹ�����еĶ�����̼��ˮ��������CӰ��ʵ����֤��
��ʵ�����������֪�������Ʊ�Ϊ��ɫ���壬����ͭ������ɫ֤����ˮ���ɣ�֤�������������Ʒ�Ӧ�����������ƣ�
��� �⣺��1���ٹ������ƺ�ˮ��Ӧ�������������Ǽ������̪��죻��ɫ��ȥ�Ŀ���ԭ���ǹ������ƺ�ˮ��Ӧ���ɵĹ���������������ԣ���������ɫ���ʣ�
�ʴ�Ϊ���������ƺ�ˮ��Ӧ���ɼ��������ƣ���Ӧ���ɵ�H2O2����Ư�����ã�
�ڹ��������ڶ��������������ֽ�����ˮ����������Ӧ�Ļ�ѧ����ʽΪ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����
�ʴ�Ϊ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����
��2���ٷ���װ��ͼ��ʵ�鲽���֪��ʢ���������Ϊ����©����Bװ�������������е��������壬��ȥ�����е�ˮ�����ȣ�
�ʴ�Ϊ������©�������������е��������壻
�������ǿ�ȼ��������п�����ȼ������ը���鴿��ֹ������������ϼ��ȱ�ը��
�ʴ�Ϊ����ֹ������������ϼ��ȱ�ը��
��Dװ���Ƿ�ֹ�����еĶ�����̼��ˮ��������CӰ��ʵ����֤��
�ʴ�Ϊ����ֹ�����еĶ�����̼��ˮ��������Cװ�ú������Ʒ�ӦӰ��ʵ����֤��
��ʵ�����������֪�������Ʊ�Ϊ��ɫ���壬����ͭ������ɫ֤����ˮ���ɣ�֤�������������Ʒ�Ӧ�����������ƣ���Ӧ�Ļ�ѧ����ʽΪNa2O2+H2$\frac{\underline{\;\;��\;\;}}{\;}$2NaOH��
�ʴ�Ϊ�������������Ʒ�Ӧ�����������ƣ�Na2O2+H2$\frac{\underline{\;\;��\;\;}}{\;}$2NaOH��
���� ���⿼�����������ʵ�ʵ����֤�ͷ����жϣ�ʵ�鲽�����Ʒ�����ע�����⣬�����������ʺ�ʵ����������ǽ���ؼ�����Ŀ�Ѷ��еȣ�

| A�� | H2SO4��K��HCl | B�� | Cl2��Al��H2 | C�� | NO2��Na��Br2 | D�� | O2��SO2��H2O |
| A�� | �����Һ����ˮ�������c��OH-���T10-8 mol•L-1 | |
| B�� | c��Na+���Tc��X-��+c��HX��=0.1mol•L-1 | |
| C�� | c��Na+��-c��X-���T9.9��10-7mol•L-1 | |
| D�� | c��OH-��-c��HX���Tc��H+��=1��10-8mol•L-1 |
| A�� | 7.8gNa2S��Na2O2�Ĺ��������к��е���������ĿΪ0.1NA | |
| B�� | ��ͭ���缫���CuSO4��Һ�ķ�Ӧ����ʽ��2Cu2++2H2O$\frac{\underline{\;���\;}}{\;}$2Cu+O2��+4H+ | |
| C�� | ��������N2��CO����ԭ������Ϊ2NA | |
| D�� | pH����2�Ĵ�����Һ�м���0.01mol/L�����ᣬ��ҺpH���С |
 �����γɶ����������NO��NO2��N2O4�ȣ�
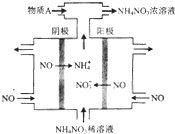
�����γɶ����������NO��NO2��N2O4�ȣ���1�����NO�Ʊ�NH4NO3���乤��ԭ����ͼ��ʾ��Ϊʹ������ȫ��ת��ΪNH4NO3���貹������A��A��NH3�������ǣ����ݷ�Ӧ��8NO+7H2O$\frac{\underline{\;���\;}}{\;}$3NH4NO3+2HNO3��������������࣬�貹��NH3��
��2��ʵ���ҿ���NaOH��Һ����NO2����ӦΪ2NO2+2NaOH=NaNO3+NaNO2+H2O����0.2mol NaOH��ˮ��Һ��0.2mol NO2ǡ����ȫ��Ӧ��1L��ҺA����ҺBΪ0.1mol/L��CH3COONa��Һ��������Һ��c��NO3?����c��NO2?����c��CH3COO?���ɴ�С��˳��Ϊc��NO3-����c��NO2-����c��CH3COO-������֪HNO2�ĵ��볣��Ka=7.1��10-4mol/L��CH3COOH�ĵ��볣��Ka=1.7��10-5mol/L������ʹ��ҺA����ҺB��pH��ȵķ�����bc��
a������ҺA�м�����ˮ b������ҺA�м�����NaOH
c������ҺB�м�����ˮ d������ҺB�м�����NaOH
��3��100��ʱ����0.400mol ��NO2�������2L��յ��ܱ������У�������Ӧ2NO2��g��?N2O4��g����H��0��ÿ��һ��ʱ��ͶԸ������ڵ����ʽ��з������õ����±���ʾ���ݣ�
| ʱ��/s | 0 | 20 | 40 | 60 | 80 |
| n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
��������ͬ�����£������������������N2O4���壬�ﵽ����ͬ����ƽ��״̬����N2O4����ʼŨ����0.1mol/L������ӷ���N2O4��ƽ��ʱ��Ҫ80s����ﵽƽ��ʱ������������ת����Ϊ60%��
| A�� | Mg2+��Cl-��Na+��NO3- | B�� | K+��Na+��NO3-��HCO3- | ||
| C�� | Na+��K+��Cl-��NO3- | D�� | Na+��Cl-��AlO2-��SO42- |
I����֪��2CO��g��+O2��g���T2CO2��g������H=-566kJ•mol-1
2Fe��s��+$\frac{3}{2}$O2��g���TFe2O3��s������H=-825.5kJ•mol-1
��Ӧ��Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g������H=-23.5 kJ•mol-1��
��Ӧ $\frac{1}{3}$Fe2O3��s��+CO��g��?$\frac{2}{3}$Fe��s��+CO2��g����1000���ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol����Ӧ����l0min��ﵽƽ�⣮
��1��CO��ƽ��ת����=60%��
��2�������CO��ƽ��ת���ʣ��ٽ�Fe2O3��ת�����ɲ�ȡ�Ĵ�ʩ��d��
a����߷�Ӧ�¶� b������Ӧ��ϵ��ѹǿ c��ѡȡ���ʵĴ��� d����ʱ���ջ��Ƴ�����CO2 e�������ʯ��ʹ����ƽ���������ֽӴ�
��¯���������ķ����е�CO�ɽ��л��գ�ʹ����һ�������º�H2��Ӧ�Ʊ��״���
CO��g��+2H2��g��?CH3OH��g���������ͼʾ�ش��������⣺
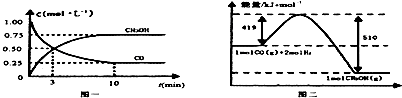
��1���ӷ�Ӧ��ʼ��ƽ�⣬��H2Ũ�ȱ仯��ʾƽ����Ӧ����v��H2��=0.15mol/��L•min����
��2�������¶Ⱥ�������ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���÷�Ӧ�ﵽƽ��ʱ���й����������
�����й�ϵ��ȷ����ADE��
| ���� | ��Ӧ��Ͷ����� | ��Ӧ��� ת���� | CH3OH��Ũ�� | �����仯 ��Q1��Q2��Q3������0�� |
| �� | 1mol CO��2mol H2 | ��1 | c1 | �ų�Q1kJ���� |
| �� | 1mol CH3OH | ��2 | c2 | ����Q2kJ���� |
| �� | 2mol CO��4mol H2 | ��3 | c3 | �ų�Q3kJ���� |
E���÷�Ӧ������1mol CH3OH����ų���Q1+Q2����kJ����
��3������һ����ɱ���ܱ������г���l molCO��2molH2��1molCH3OH���ﵽƽ��ʱ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6������÷�Ӧ����������������桱����Ӧ�����ƶ���
��4���״�������������ȼ�ϵ�أ��õ���ö�Ķ��Ե缫����Ũ����������Һ��д���õ�صĸ�����ӦʽCH3OH-6e-+8OH-=CO32-+6H2O��