��Ŀ����
9�������������ؾ���{K3[Fe��C2O4��3]•xH2O}��һ�ֹ������ϣ�Ϊ�ⶨ�þ��������ĺ�����ijʵ��С����������ʵ�飺����һ������4.00g�����������ؾ��壬���Ƴ�250mL��Һ��
�������ȡ������Һ25.00mL����ƿ�У���ϡH2SO4�ữ���μ�KMnO4��Һ�������ǡ��ȫ�������ɶ�����̼��ͬʱ��MnO4-����ԭ��Mn2+����Ӧ�����Һ�м���һС��п�ۣ���������ɫ�պ���ʧ�����ˣ�ϴ�ӣ������˼�ϴ��������Һ�ռ�����ƿ�У���ʱ����Һ�Գ����ԣ�
����������0.010mol/L KMnO4��Һ�ζ������������Һ���յ㣬����KMnO4��Һ20.02mL���ζ���MnO4-����ԭ��Mn2+��
�ظ���������������������ζ�����0.010mol/L KMnO4��Һ19.98mL��
��ش��������⣺
��1��������������������Һ�IJ������������ǣ��������ܽ⡢ת�ơ�ϴ�Ӳ�ת�ơ����ݡ�ҡ�ȣ�
��2������п�۵�Ŀ���ǽ�Fe3+ǡ�û�ԭ��Fe2+��ʹFe2+�ڲ���������KMnO4����������ԭ��Ӧ��
��3��д���������з�����Ӧ�����ӷ���ʽ��5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O��
��4��ʵ���øþ�����������������Ϊ14%���ڲ�����У��������KMnO4��Һ�������������õ�������ƫ�ߣ���ѡ�ƫ�͡�����ƫ�ߡ����䡱��
���� ��1����������һ�����ʵ���Ũ�ȵ���Һ�IJ��������жϣ����������ʵ���Ũ�ȵ���Һʱ��Ҫ������������������ܽ����Һ��ϴ�ӡ������ݡ�ҡ�ȵȲ��裻
��2��п������Fe3+��Ӧ������п�۵�Ŀ���ǽ�Fe3+ǡ�û�ԭ��Fe2+��
��3��������KMnO4��Һ�ζ��������������������������ӣ��ݴ���д���ӷ���ʽ��
��4���������ӷ���ʽ���㣬n��Fe��=5n��MnO4-����������������������=$\frac{m������}{m���ܣ�}$��100%���㣬���ڲ�����е������Ը��������Һ���㣬����в��ֲ��������δ���������ڲ��������������������Ը��������Һ����ƫ�Ӷ�����������������࣬����ƫ�ߣ�
��� �⣺��1�����������ʵ���Ũ�ȵ���Һʱ��Ҫ������������������ܽ����Һ��ϴ�ӡ������ݡ�ҡ�ȵȲ��裬�ʴ�Ϊ���ܽ⣻���ݣ�
��2������п�۵�Ŀ���ǽ�Fe3+ǡ�û�ԭ��Fe2+���ʴ�Ϊ����Fe3+ǡ�û�ԭ��Fe2+��ʹFe2+�ڲ���������KMnO4����������ԭ��Ӧ��
��3���ڲ�������KMnO4��Һ�ζ��������������������������ӣ����������ӷ�ӦΪ��5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O���ʴ�Ϊ��5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O��
��4�����ݲ������е����ӷ�Ӧ��֪��n��Fe��=5n��MnO4-��=5��19.98��10-3��0.01 mol•L-1��10=0.00999mol��m��Fe��=56 g•mol-1��0.0099mol=0.5594g��������������������=$\frac{0.5594g}{4g}$��100%=14%�����ڲ�����е������Ը��������Һ���㣬����в��ֲ��������δ���������ڲ��������������������Ը��������Һ����ƫ�Ӷ�����������������࣬����ƫ�ߣ��ʴ�Ϊ��14%��ƫ�ߣ�
���� ���⿼���Ϊ�ۺϣ��漰����Һ�����ơ��ζ��ͽᾧ�Ȳ�����ע�����ʵ��֪ʶ�Ļ��ۣ�����ʵ�鲽�衢ԭ����ע����������⣬��Ŀ�Ѷ��еȣ�

 ÿ�α���ϵ�д�
ÿ�α���ϵ�д�| A�� | ��Ӧ�ﵽƽ��������������䣬ֻ�ı�ѹǿ��ƽ�ⲻ�ƶ� | |
| B�� | ������Ӧ�����е�ƽ����Է����������� | |
| C�� | ��λʱ���ڷ�Ӧ��Ũ�ȵļ��ٵ���������Ũ�ȵ����� | |
| D�� | ����ǰ10s��B������xmol������ǰ20s��A����С��2xmol |
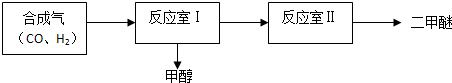
��Ӧ�Ң�CO��g��+2H2��g���TCH3OH��g��
��Ӧ�Ң�2CH3OH��g���TCH3OCH3��g��+H2O��g��
��1������߷�Ӧ�Ң���CO��ת���ʣ����Բ�ȡ�ķ�������������Ũ�ȡ����Ϸ�����״�����ѹ��
��2����Ӧ�Ң���10L�����йط�Ӧ�������£�
| ��� | �¶ȣ���C�� | ��ʼŨ�ȣ�mol•L-1�� | ƽ��Ũ�ȣ�mol•L-1�� | ||||
| CO | H2 | CH3OH | CO | H2 | CH3OH | ||
| �� | T | 1 | 3 | 0 | 0.2 | 1.4 | 0.8 |
| �� | T | 1.5 | 4.6 | 0.1 | b1 | b2 | b3 |
| �� | T+30 | 1 | 3 | 0 | 0.25 | 1.5 | 0.75 |
���жϣ�$\frac{{b}_{3}}{{b}_{1}}$��4�����������������=������
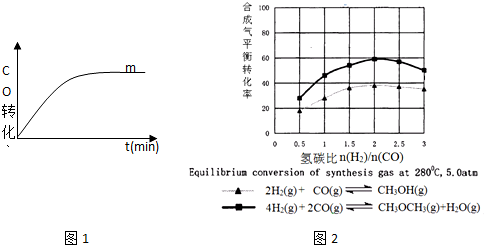
��3��ͼ2��ʾ�״�������������������̼��$\frac{n��{H}^{2}��}{n��CO��}$�ı仯�������ͼ�п��Եõ��Ľ�����C��
A�������̼�ȿ��Լӿ췴Ӧ����
B�������̼�ȿ������������ת����
C��������ʽϵ����Ͷ��ʱ�״������������������
D������ͬһ��Ӧ��̼��Խ��������Ũ��Խ��
��4����֪ij�¶��������Ȼ�ѧ����ʽ��CO��g��+2H2��g���TCH3OH��g����H1=-100.46kJ•mol-1
2CH3OH��g���TCH3OCH3��g��+H2O��g����H2=-20.59kJ•mol-1����2CO��g��+4H2��g���TCH3OCH3��g��+H2O��g����H3=-221.51kJ•mol-1��
| A�� | 4.2 g CO | B�� | 6.6 g CO2 | C�� | 8 g SO2 | D�� | 9.8 g H2SO4 |
| A�� | Al2��SO4��3�T2Al3++3SO42- | B�� | FeCl2�TFe2++3Cl- | ||
| C�� | H2SO4�TH2++SO42- | D�� | Ca��OH��2�TCa2++2��OH-�� |
 �������˲����㣬�Ҿ���һ����Σ���ԣ�Ŀǰ��������������Խ��������Ʒ���������ش�
�������˲����㣬�Ҿ���һ����Σ���ԣ�Ŀǰ��������������Խ��������Ʒ���������ش�