题目内容
20.有关图的说法不正确的是( )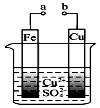
| A. | 构成原电池时Cu极反应为:Cu2++2e-=Cu | |
| B. | 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 | |
| C. | 要使Fe极不被腐蚀,Cu片换Zn片或将a与直流电源的负极相连 | |
| D. | a和b分别连接直流电源正、负极,Fe片上有气体产生 |
分析 A、构成原电池时Cu极为正极发生还原反应,反应为Cu2++2e-=Cu;
B、连接发生铁发生电化学腐蚀,不连接铁发生化学腐蚀;
C、电解时,阳极上失电子,金属阴极被保护,或者将铜变成比铁活泼的金属;
D、a和b分别连接直流电源正、负极,则铁是阳极,铁本身放电生成亚铁离子.
解答 解:A、构成原电池时Cu极为正极发生还原反应,反应为Cu2++2e-=Cu,故A正确;
B、连接发生铁发生电化学腐蚀,不连接铁发生化学腐蚀,所以铁片均会溶解,溶液从蓝色逐渐变成浅绿色,故B正确;
C、电解时,阳极上失电子,金属阴极被保护,或者将铜变成比铁活泼的金属,故C正确;
D、a和b分别连接直流电源正、负极,则铁是阳极,铁本身放电生成亚铁离子,故D错误;
故选D.
点评 本题考查了原电池原理和电解池原理,电化反应的原理来分析解答,比较容易.

练习册系列答案
相关题目
10.下列说法中正确的是(NA代表阿伏加德罗常数的值)( )
| A. | 7.1 g氯气和7.1 g氯水所含的分子数都是0.1 NA | |
| B. | 36.5 g氯化氢和36.5 g盐酸所含的分子数都是NA | |
| C. | 1 mol Mg转化为MgCl2必定有NA个Cl2分子参加了反应 | |
| D. | 1 mol Fe转化为Fe3+失去的电子数为3NA |
11.0.1mol/L的HCl和0.1mol/L的CH3COOH溶液相比较,下列说法不正确的是( )
| A. | 含H+的物质的量,盐酸大于醋酸 | |
| B. | 分别于锌反应,产生H2的物质的量不一定相等 | |
| C. | 分别于镁反应,反应速率盐酸大于醋酸 | |
| D. | H+的物质的量浓度,盐酸大于醋酸 |
8.下列离子方程式正确的是( )
| A. | SO2与酸性KMnO4溶液的反应:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+ | |
| B. | 稀硫酸和氢氧化钡溶液反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | 硝酸银溶液中滴加过量氨水:Ag++NH3•H2O═AgOH↓+NH4+ | |
| D. | 石灰水与过量碳酸氢钠溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
15.下列反应的离子方程式正确的是( )
| A. | 氢氧化钙溶液与少量碳酸氢镁溶液反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| B. | 向次氯酸钙溶液中通入少量SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO | |
| C. | Ca(HCO3)2溶液中加入过量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 硫酸亚铁的酸性溶液中加入H2O2溶液:Fe2++H2O2+2H+═Fe3++2H2O |
5.有物质的量浓度均为0.1mol•L-1 的①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25mL,下列说法正确的是( )
| A. | 3种溶液pH的大小顺序是 ③>②>① | |
| B. | 若将3种溶液稀释相同倍数,pH变化最大的是① | |
| C. | 若分别加入25mL 0.1mol•L-1盐酸后,pH最小的是② | |
| D. | 若升高温度,则③的pH不变 |
12.在强碱性溶液中,下列各组离子能在同一溶液里大量共存的是( )
| A. | Na+、Al3+、Cl- | B. | K+、H+、SO42- | C. | Na+、HCO3-、NO3- | D. | K+、Na+、AlO2- |
4.标准状况下VL氨气溶解在1L水中,所得溶液的密度为ρ g/ml,质量分数为ω,物质浓度为c mol/L,则下列关系中正确的是( )
| A. | c=$\frac{Vρ}{17V+22400}$ | B. | ω=$\frac{17c}{100ρ}$ | ||
| C. | ω=$\frac{17V}{17V+22400}$ | D. | ρ=$\frac{17V+22400}{22.4+22.4V}$ |
5.将溶质的质量分数为10%的KOH溶液加热蒸发掉100g水后,得到溶质的质量分数为35%的溶液50mL,此时溶液的物质的量浓度为( )
| A. | 5mol•L-1 | B. | 3.25mol•L-1 | C. | 7mol•L-1 | D. | 6.25mol•L-1 |