题目内容
7.下列物质是纯净物的是( )| A. | 新制氯水 | B. | 液氯 | C. | 漂白粉 | D. | 盐酸 |
分析 混合物:由两种或多种物质混合而成的物质;
纯净物:由一种物质组成的物质.
解答 解:A.新制的氯水是氯气的水溶液,属于混合物,故A错误;
B.液氯是单质,属于纯净物,故B正确;
C.漂白粉的主要成分是次氯酸钙和氯化钙,属于混合物,故C错误;
D.盐酸是氯化氢的水溶液,属于混合物,故D错误,
故选B.
点评 本题考查纯净物的概念,难度不大.根据纯净物的定义判断即可.

练习册系列答案
相关题目
6.某有机物A的结构简式如图所示,有关叙述中正确的是( )
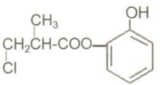

| A. | 有机物A与浓硫酸混合加热,可以发生消去反应 | |
| B. | 1molA和足量的H2发生加成反应,最多可以消耗4molH2 | |
| C. | 1molA和足量NaOH溶液发生反应,最多可以消耗 4molNaOH | |
| D. | 有机物A不能在稀硫酸下水解 |
18.下列熔、沸点高低的比较不正确的是( )
| A. | 金刚石>碳化硅>晶体硅 | B. | 邻羟基苯甲酸>对羟基苯甲酸 | ||
| C. | 纯铁>生铁 | D. | MgO>MgCl2 |
15.下列说法正确的是( )
| A. | 氢气的燃烧热为285.5KJ/mol,则电解水的热化学方程式为2H2O(l)$\frac{\underline{\;电解\;}}{\;}$ 2H2(g)+O2(g)△H=+285.5KJ/mol | |
| B. | 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3KJ/mol 则稀H2SO4溶液和稀Ba(OH)2溶液反应的反应热△H=2×(-57.3)KJ/mol | |
| C. | 在CO2中,Mg燃烧生成MgO和C,该反应中化学能全都转化为热能 | |
| D. | 已知AX3的熔点和沸点分别为一93.6℃和76℃,AX5的熔点为167℃.室温时AX3与气体X2反应生成1 mol AX5,放出热量123.8 KJ/mol.该反应的热化学方程式为AX3(l)+X2(g)═AX5(s)△H=一123.8 KJ/mol |
12.将氯化铝溶液加热蒸干、灼烧,最后所得固体的主要成分是( )
| A. | 水合三氯化铝 | B. | 氢氧化铝 | C. | 无水氯化铝 | D. | 氧化铝 |
19.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 含NA个N2和O2的混合气体中质子数不可能是15NA | |
| B. | 1 L 1 mol•L-1的CH3COONa溶液中CH3COOH和CH3COO-的总数为NA | |
| C. | 58g 分子式为C4H10的有机物中,所含有的甲基数一定为2NA | |
| D. | NA个CH4和NA个Cl2光照下充分反应,被取代的氢原子数为2NA |
16.在下列指定条件的溶液中,一定能大量共存的离子组是( )
| A. | K2S溶液中:SO42-、K+、Cl-、Cu2+ | |
| B. | 无色溶液中:Fe2+、Na+、ClO-、Cl- | |
| C. | 室温下,$\frac{KW}{c({H}^{+})}$=0.1mol•L-1的溶液中:Na+、K+、SiO32-、NO3- | |
| D. | 滴入KSCN溶液显红色的溶液中:K+、Na+、SO42-、C6H5OH |