题目内容
19.下列说法不正确的是( )①为了除去锅炉水垢中的CaSO4,可先用碳酸钠溶液处理,再用盐酸处理
②将硫酸铜晶体放入浓硫酸中属于物理变化
③强氧化剂与强还原剂混合,一定能发生氧化还原反应
④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
| A. | ①④ | B. | ①④⑤ | C. | ①②③④ | D. | ②③④⑤ |
分析 ①加碳酸钠,发生沉淀的转化生成碳酸钙,碳酸钙溶于盐酸;
②硫酸铜晶体放入浓硫酸中,蓝色表为白色;
③强氧化剂与强还原剂混合不一定反应,如高锰酸钾与氢气;
④离子化合物中含离子,熔融态离子可自由移动;
⑤导电能力与离子浓度、离子电荷有关.
解答 解:①加碳酸钠,发生沉淀的转化生成碳酸钙,碳酸钙溶于盐酸,则除去锅炉水垢中的CaSO4,可先用碳酸钠溶液处理,再用盐酸处理,故正确;
②硫酸铜晶体放入浓硫酸中,蓝色表为白色,五水硫酸铜转化为硫酸铜,发生化学变化,故错误;
③强氧化剂与强还原剂混合不一定反应,如高锰酸钾与氢气、过氧化钠与钠等均不反应,故错误;
④离子化合物中含离子,熔融态离子可自由移动,可导电,固态的离子化合物不导电,故错误;
⑤导电能力与离子浓度、离子电荷有关,与电解质的强弱无关,故错误;
故选D.
点评 本题考查较综合,涉及难溶电解质的溶解平衡、氧化还原反应、离子化合物及溶液导电性,综合性较强,把握化学反应原理为解答的关键,侧重分析与应用能力的考查,注意硫酸铜晶体转化为硫酸铜的过程为易错点,题目难度不大.

练习册系列答案
相关题目
12.下列推断正确的是( )
| A. | 1 mol Na2O2与水反应,转移电子1 mol | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应的产物也相同 | |
| C. | 钠能与氧气和水反应,钠暴露在空气中最终的产物是NaOH | |
| D. | 将Na2O2加入酚酞试液中,得到红色溶液 |
14.由反应物X 转化为Y 和Z的能量变化如图所示.下列说法正确的是( )


| A. | 由X→Y反应的△H=E5-E2 | B. | 由X→Z反应的△H>0 | ||
| C. | 降低压强有利于提高Y的产率 | D. | 升高温度有利于提高Z的产率 |
4.反应过程中A(g)、B(g)、C(g)物质的量变化如图所示,根据图中所示判断下列说法正确的是( )
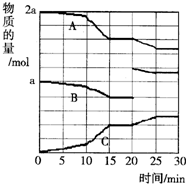

| A. | 10~15 min可能是扩大了容器体积 | B. | 10~15 min可能是降低了温度 | ||
| C. | 20 min时可能是缩小了容器体积 | D. | 20 min时可能是增加了B的量 |
11.侯氏制碱法与索氏氨碱法相比较,其优点是( )
| A. | 原料便宜 | B. | CO2参与循环,低碳环保 | ||
| C. | 产生了更多的氯化钙 | D. | 原料利用率高,节省设备 |
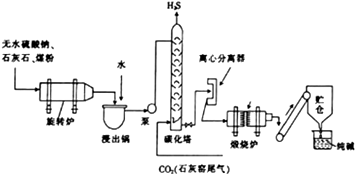 历史上路布兰法生产纯碱的工艺流程如图所示.
历史上路布兰法生产纯碱的工艺流程如图所示. 实验室需要0.1mol•L-1NaOH溶液500mL,根据溶液的配制情况,回答下列问题:
实验室需要0.1mol•L-1NaOH溶液500mL,根据溶液的配制情况,回答下列问题: