题目内容
14.由反应物X 转化为Y 和Z的能量变化如图所示.下列说法正确的是( )
| A. | 由X→Y反应的△H=E5-E2 | B. | 由X→Z反应的△H>0 | ||
| C. | 降低压强有利于提高Y的产率 | D. | 升高温度有利于提高Z的产率 |
分析 由图象可知2X(g)≒3Y(g)为吸热反应,而2X(g)≒Z(g)为放热反应,反应热等于反应物的总能量-生成物的总能量,结合温度、压强对平衡移动的影响解答该题.
解答 解:A.根据化学反应的实质,由X→Y反应的△H=E3-E2,故A错误;
B.由图象可知,反应物的总能量高于生成物的总能量,该反应为放热反应,即由反应的△H<0,故B错误;
C.根据化学反应2X(g)≒3Y(g),该反应是气体系数和增加的可逆反应,降低压强,平衡正向移动,有利于提高Y的产率,故C正确;
D.由B分析可知,该反应为放热反应,升高温度,平衡逆向移动,Z的产率降低,故D错误;
故选C.
点评 本题考查了化学反应中能量的变化图,为2016年海南高考题,侧重于学生的分析能力的考查,注意把握图象的分析,注意根据反应物的总能量与生成物的总能量进行比较,题目较简单.

练习册系列答案
相关题目
7.下列做法正确的是( )
| A. | 为了使火腿肠颜色更鲜红,可多加一些亚硝酸钠 | |
| B. | 为了使婴儿对食品有浓厚兴趣,我们可以在婴儿食品中加少量着色剂 | |
| C. | 服用阿斯匹林后出现胃肠道反应是中毒的表现,应立即停药 | |
| D. | 为保证人体所需足够蛋白质我们要多吃肉,少吃蔬菜和水果 |
9. 铁及其化合物在工农业生产、科学研究等方面具有广泛用途.回答下列问题:
铁及其化合物在工农业生产、科学研究等方面具有广泛用途.回答下列问题:
(1)在FeCl3饱和溶液中滴加饱和纯碱溶液可观察到有红褐色沉淀和气泡生成,写出该反应的离子方程式:2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(2)工业上应用铁矿石冶炼金属铁时涉及的反应有:
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H1=-24.8kJ•mol-1
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H2=-47.2kJ•mol-1
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H3=+640.5kJ•mol-1
写出CO还原FeO的热化学方程式:CO(g)+FeO(s)=Fe(s)+CO2(g)△H=-218.0kJ/mol.
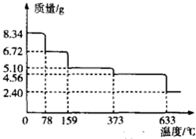
(3)绿矾(FeSO4•7H2O)在受热条件下不稳定,易发生分解.现取绿矾样品8.34g,在隔绝空气的条件下加热,样品质量随着温度的变化曲线如图所示.
159℃时的固体物质的化学式为FeSO4•H2O;633℃时分解除生成固体物质外,还有两种气体物质,且这两种气体物质的密度之比为4:5,则633℃时分解的化学方程式为2FeSO4$\frac{\underline{\;633℃\;}}{\;}$Fe2O3+SO2↑+SO3↑.
(4)已知密闭容器中发生反应:Fe(S)+CO2(g)?FeO(s)+CO(g)△H>0.测得在不同温度下,该反应的平衡常数随温度的变化数据如表所示.
①该反应的化学平衡常数表达式K=$\frac{C(CO)}{C(C{O}_{2})}$;上述表格中的x、y的数值可能是a(填字母).
a.1.47、2.40 b.2.40、1.47 c.0.64、0.48d.0.48、0.64
②500℃时,在容积为2L的密闭容器中放入2mol铁粉和2mol CO2,若测得10min时反应达到平衡状态,则0~10min内的平均反应速率v(CO2)=0.05mol/(L•min).
③800℃时,在反应达到平衡状态后,要使反应速率减小且平衡逆向移动,可采取的措施有减小二氧化碳的物质的量(或者降低温度)(写出一种即可).
(5)高铁酸钠(Na2FeO4)能有效地杀灭水中的病菌和病毒,在对水的消毒和净化过程中,不产生任何对人体有害的物质,其消毒和除污效果比含氯消毒剂要好.高铁酸钠的制备方法之一是电解:Fe+2H2O+2OH-$\frac{\underline{\;通电\;}}{\;}$FeO42-+3H2↑,电解质溶液选用NaOH溶液.该电解池的阳极反应式为Fe+8OH--6e-=FeO42-+4H2O.
 铁及其化合物在工农业生产、科学研究等方面具有广泛用途.回答下列问题:
铁及其化合物在工农业生产、科学研究等方面具有广泛用途.回答下列问题:(1)在FeCl3饱和溶液中滴加饱和纯碱溶液可观察到有红褐色沉淀和气泡生成,写出该反应的离子方程式:2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(2)工业上应用铁矿石冶炼金属铁时涉及的反应有:
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H1=-24.8kJ•mol-1
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H2=-47.2kJ•mol-1
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H3=+640.5kJ•mol-1
写出CO还原FeO的热化学方程式:CO(g)+FeO(s)=Fe(s)+CO2(g)△H=-218.0kJ/mol.
(3)绿矾(FeSO4•7H2O)在受热条件下不稳定,易发生分解.现取绿矾样品8.34g,在隔绝空气的条件下加热,样品质量随着温度的变化曲线如图所示.
159℃时的固体物质的化学式为FeSO4•H2O;633℃时分解除生成固体物质外,还有两种气体物质,且这两种气体物质的密度之比为4:5,则633℃时分解的化学方程式为2FeSO4$\frac{\underline{\;633℃\;}}{\;}$Fe2O3+SO2↑+SO3↑.
(4)已知密闭容器中发生反应:Fe(S)+CO2(g)?FeO(s)+CO(g)△H>0.测得在不同温度下,该反应的平衡常数随温度的变化数据如表所示.
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | x | Y |
a.1.47、2.40 b.2.40、1.47 c.0.64、0.48d.0.48、0.64
②500℃时,在容积为2L的密闭容器中放入2mol铁粉和2mol CO2,若测得10min时反应达到平衡状态,则0~10min内的平均反应速率v(CO2)=0.05mol/(L•min).
③800℃时,在反应达到平衡状态后,要使反应速率减小且平衡逆向移动,可采取的措施有减小二氧化碳的物质的量(或者降低温度)(写出一种即可).
(5)高铁酸钠(Na2FeO4)能有效地杀灭水中的病菌和病毒,在对水的消毒和净化过程中,不产生任何对人体有害的物质,其消毒和除污效果比含氯消毒剂要好.高铁酸钠的制备方法之一是电解:Fe+2H2O+2OH-$\frac{\underline{\;通电\;}}{\;}$FeO42-+3H2↑,电解质溶液选用NaOH溶液.该电解池的阳极反应式为Fe+8OH--6e-=FeO42-+4H2O.
19.下列说法不正确的是( )
①为了除去锅炉水垢中的CaSO4,可先用碳酸钠溶液处理,再用盐酸处理
②将硫酸铜晶体放入浓硫酸中属于物理变化
③强氧化剂与强还原剂混合,一定能发生氧化还原反应
④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
①为了除去锅炉水垢中的CaSO4,可先用碳酸钠溶液处理,再用盐酸处理
②将硫酸铜晶体放入浓硫酸中属于物理变化
③强氧化剂与强还原剂混合,一定能发生氧化还原反应
④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
| A. | ①④ | B. | ①④⑤ | C. | ①②③④ | D. | ②③④⑤ |
6.硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
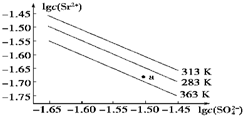

| A. | 温度一定时,Ksp(SrSO4)随c(SO42- )的增大而减小 | |
| B. | 三个不同温度中,313 K时Ksp(SrSO4)最大 | |
| C. | 283 K时,图中a点对应的溶液是饱和溶液 | |
| D. | 283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液 |
3. 某同学Cr2O72-(aq)+H2O(l)?2CrO42-(aq)+2H+(aq)△H=+13.8kJ/mol
某同学Cr2O72-(aq)+H2O(l)?2CrO42-(aq)+2H+(aq)△H=+13.8kJ/mol
(橙色) (黄色)
研究浓度对化学平衡的影响,下列说法正确的是( )
已知:
现象:
1:待试管b中颜色不变后与试管a比较,溶液颜色变浅.
2:滴加浓硫酸,试管c温度略有升高,溶液颜色与试管a相比,变深.
 某同学Cr2O72-(aq)+H2O(l)?2CrO42-(aq)+2H+(aq)△H=+13.8kJ/mol
某同学Cr2O72-(aq)+H2O(l)?2CrO42-(aq)+2H+(aq)△H=+13.8kJ/mol(橙色) (黄色)
研究浓度对化学平衡的影响,下列说法正确的是( )
已知:
现象:
1:待试管b中颜色不变后与试管a比较,溶液颜色变浅.
2:滴加浓硫酸,试管c温度略有升高,溶液颜色与试管a相比,变深.
| A. | 该反应是一个氧化还原反应 | |
| B. | 待试管b中溶液颜色不变的目的是使Cr2O72-完全反应 | |
| C. | 该实验不能证明减小生成物浓度,平衡正向移动 | |
| D. | 试管c中的现象说明影响平衡的主要因素是温度 |
4.下列是常用的中和胃酸的药物:
估算10片胃舒平和5片达喜,含铝的物质的量较多的是10片胃舒平.
| 药名 | 胃舒平 | 达喜 |
| 有效成分的化学式 | Al(OH)3 | Al2Mg6(OH)16CO3•4H2O |
| 相对分子质量 | 78 | 530 |
| 每片含有效成分的药量 | 0.245g | 0.5g |