题目内容
4.反应过程中A(g)、B(g)、C(g)物质的量变化如图所示,根据图中所示判断下列说法正确的是( )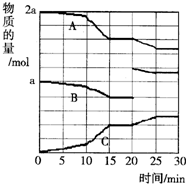
| A. | 10~15 min可能是扩大了容器体积 | B. | 10~15 min可能是降低了温度 | ||
| C. | 20 min时可能是缩小了容器体积 | D. | 20 min时可能是增加了B的量 |
分析 A.10~15min未到达平衡,且改变条件,速率增大,反应进行向正反应进行,可能为使用催化剂或升高温度或增大压强;
B.10~15min,反应速率增大,如果降低温度,反应速率会减小;
C.20min时若缩小了容器体积,则20min时B的物质的量不会变化;
D.20min时A、C的物质的量不变,B的物质的量增大,反应向正反应移动,应增大B的物质的量,可能是增加了B的量.
解答 解:A.根据图象可知,10~15min未到达平衡,且改变条件后,反应速率都增大,反应向着正反应方向进行,可能为使用催化剂或升高温度或增大压强,不可能扩大了容器容积(减小压强),故A正确;
B.10~15min未到达平衡,且改变条件,反应速率都增大,若降低温度反应速率减慢,故B错误;
C.20min时A、C的物质的量不变,B的物质的量增大,反应向正反应移动,应增大B的物质的量;如果缩小容器体积,则20min时B的物质的量不会变化,故C错误;
D.20min时A、C的物质的量不变,B的物质的量增大,反应向正反应移动,应该是增大了B的物质的量,故D正确;
故选D.
点评 本题考查了物质的量或浓度随时间变化的曲线,题目难度中等,明确图象曲线变化的含义为解答关键,注意熟练掌握化学平衡及其影响,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
17.有关金属腐蚀的论述,正确的是( )
①金属的腐蚀一定伴有电流产生
②纯银器表面在空气中因化学腐蚀渐渐变暗
③可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
④发生化学能转变为电能的腐蚀时较活泼的金属总是作正极而被腐蚀
⑤发生电化学腐蚀时都有能量的转变,且被腐蚀的金属总是失电子
⑥当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
⑦海轮外壳连接锌块以保护外壳不受腐蚀.
①金属的腐蚀一定伴有电流产生
②纯银器表面在空气中因化学腐蚀渐渐变暗
③可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
④发生化学能转变为电能的腐蚀时较活泼的金属总是作正极而被腐蚀
⑤发生电化学腐蚀时都有能量的转变,且被腐蚀的金属总是失电子
⑥当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
⑦海轮外壳连接锌块以保护外壳不受腐蚀.
| A. | ②③⑤⑦ | B. | ①②③⑥⑦ | C. | ①②④⑦ | D. | ②③⑤⑥⑦ |
15.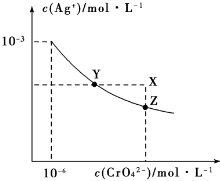 t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
 t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A. | 加热蒸发饱和Ag2CrO4溶液再恢复到t℃,可使溶液由Y点变到Z点 | |
| B. | 在X点没有Ag2CrO4沉淀生成,则此时温度低于t℃ | |
| C. | 向饱和Ag2CrO4溶液中加入少量AgNO3固体,可使溶液由Z点到Y点 | |
| D. | 在t℃时,Ag2CrO4的Ksp为1×10-9 |
19.下列说法不正确的是( )
①为了除去锅炉水垢中的CaSO4,可先用碳酸钠溶液处理,再用盐酸处理
②将硫酸铜晶体放入浓硫酸中属于物理变化
③强氧化剂与强还原剂混合,一定能发生氧化还原反应
④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
①为了除去锅炉水垢中的CaSO4,可先用碳酸钠溶液处理,再用盐酸处理
②将硫酸铜晶体放入浓硫酸中属于物理变化
③强氧化剂与强还原剂混合,一定能发生氧化还原反应
④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
| A. | ①④ | B. | ①④⑤ | C. | ①②③④ | D. | ②③④⑤ |
9.在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g)?xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
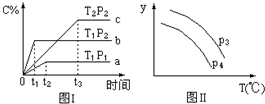

| A. | P3>P4,y轴表示B的转化率 | |
| B. | P3<P4,y轴表示B的体积分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3<P4,y轴表示混合气体的平均摩尔质量 |
16.已知Ksp(AgCl )=1.8×10-10,Ksp(AgI)=1.0×10-16.下列关于不溶物之间转化的说法中错误的是( )
| A. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于$\frac{1}{\sqrt{1.8}}$×10-11 mol•L-1 | |
| B. | 向BaCl2溶液中加入AgNO3和KI,当两种沉淀共存时,$\frac{c({I}^{-})}{c(C{l}^{-})}$=5.6×10-7 | |
| C. | AgI比AgCl更难溶于水,所以,AgCl可以转化为AgI | |
| D. | AgCl不溶于水,不能转化为AgI |
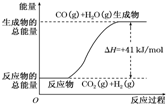 (1)已知14g N2与足量H2反应放出46kJ的热量,则该反应的热化学方程式是N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol
(1)已知14g N2与足量H2反应放出46kJ的热量,则该反应的热化学方程式是N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol →
→