题目内容
10.如图为铜锌原电池的示意图,下列有关的说法中不正确的是( )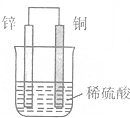
| A. | 锌片上有H2逸出 | B. | 溶液中c(H+)逐渐减小 | ||
| C. | 正极反应式:2H++2e-═H2↑ | D. | 负极反应式:Zn-2e-═Zn2+ |
分析 该原电池中,Zn易失电子作负极、Cu作正极,负极反应式为Zn-2e-═Zn2+,正极反应式为2H++2e-═H2↑,据此分析解答.
解答 解:该原电池中,Zn易失电子作负极、Cu作正极,
A.锌电极上Zn失电子生成锌离子进入溶液,正极上氢离子得电子生成氢气,所以铜片上有氢气逸出,故A错误;
B.正极上氢离子放电生成氢气,导致溶液中c(H+)逐渐减小,故B正确;
C.正极上氢离子放电生成氢气,电极反应式为2H++2e-═H2↑,故C正确;
D.负极上锌失电子发生氧化反应,电极反应式为Zn-2e-═Zn2+,故D正确;
故选A.
点评 本题考查原电池原理,为高频考点,明确正负极判断方法及各个电极上发生的反应是解本题关键,会正确书写电极反应式,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.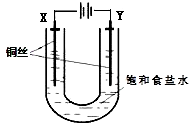 已知:Ksp(CuCl,白色)=1.2×10-6,Ksp(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-═CuCl.下列说法不正确的是( )
已知:Ksp(CuCl,白色)=1.2×10-6,Ksp(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-═CuCl.下列说法不正确的是( )
 已知:Ksp(CuCl,白色)=1.2×10-6,Ksp(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-═CuCl.下列说法不正确的是( )
已知:Ksp(CuCl,白色)=1.2×10-6,Ksp(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-═CuCl.下列说法不正确的是( )| A. | Y极发生的电极反应2H2O+2e-═2OH-+H2↑ | |
| B. | 实验开始时,X极附近出现白色浑浊 | |
| C. | 一段时间后,U形管底部形成橙黄色沉淀 | |
| D. | 电解时,Cl-移向Y极 |
3.关于有机物 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )
 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )| A. | 它的系统名称是2,4-二甲基-4-戊烯 | |
| B. | 它的分子中最多有5个碳原子在同一平面上 | |
| C. | 它与甲基环己烷互为同分异构体 | |
| D. | 有机物的一氯取代产物共有4种 |
20.下列有机物中,含有两种官能团的是( )
| A. | CH2=CHCH2Cl | B. | CH3OH | C. | Cl-C2H4-Cl | D. | Br-CH=CH-Cl |
5.下列说法正确的是( )
| A. | 活化分子间所发生的碰撞都为有效碰撞 | |
| B. | 合成氨工业中用铁触媒做催化剂能用勒夏特列原理解释 | |
| C. | 升高温度能使化学反应速率增大的主要原因是增加了单位体积内活化分子的百分数 | |
| D. | 将钢闸门与电源的正极相连,是采用了外加电流的阴极保护法 |
2.将0.02molNa分别投入到盛有100mL水、100 mL 1mol•L-1盐酸、100mL 1mol•L-1硫酸铜溶液的X、Y、Z三个烧杯中,下列有关说法错误的是( )
| A. | 三个烧杯中一定均会发生的离子反应有:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 三个烧杯中钠均在液面上剧烈反应 | |
| C. | Z烧杯中一定会有沉淀生成,但沉淀不是单质铜 | |
| D. | 三个烧杯中生成氢气的物质的量相同 |
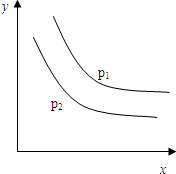
19.反应:aL(s)+bG(g)?cR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,
x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )
x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )

| A. | 上述反应是放热反应 | B. | 上述反应是吸热反应 | ||
| C. | a+b>c | D. | a+b<c |
20.下列说法正确的是( )
| A. | 润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 | |
| B. | 用惰性电极电解MgCl2溶液的离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 为验证盐桥的作用,在两个烧杯中分别盛适量硫酸亚铁铵溶液和稀酸性高锰酸钾溶液,分别插入石墨棒用导线与电流计相连,然后用装有K2SO4饱和溶液的琼脂的U型管两端插入两个烧杯中,电流计偏转,一段时间后高锰酸钾溶液褪色 | |
| D. | 嫦娥三号月球车玉兔号在进入第二个月夜休眠前,出现了机构控制异常情况,其病因或为月尘,即月球上直径小于10微米的浮尘,月尘分散在空气中形成的分散系属于胶体 |
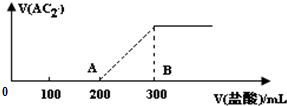 A、B、C、D、E为原子序数依次增大的五种短周期元素,A、B、C位于同一周期,C、E位于同一主族,A元素在自然界中形成的化合物种类最多,C元素的氢化物是最常用的溶剂,D元素在同周期元素中离子半径最小.请回答:
A、B、C、D、E为原子序数依次增大的五种短周期元素,A、B、C位于同一周期,C、E位于同一主族,A元素在自然界中形成的化合物种类最多,C元素的氢化物是最常用的溶剂,D元素在同周期元素中离子半径最小.请回答: ;D元素的最高价氧化物的水化物的电离方程式Al(OH)3?Al3++3OH-.
;D元素的最高价氧化物的水化物的电离方程式Al(OH)3?Al3++3OH-.