题目内容
2.将0.02molNa分别投入到盛有100mL水、100 mL 1mol•L-1盐酸、100mL 1mol•L-1硫酸铜溶液的X、Y、Z三个烧杯中,下列有关说法错误的是( )| A. | 三个烧杯中一定均会发生的离子反应有:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 三个烧杯中钠均在液面上剧烈反应 | |
| C. | Z烧杯中一定会有沉淀生成,但沉淀不是单质铜 | |
| D. | 三个烧杯中生成氢气的物质的量相同 |
分析 钠密度小于水,钠投入溶液中,发生的反应实质是钠与酸或者水电离产生的氢离子的反应,溶液中氢离子浓度越大,反应越剧烈,生成的氢氧化钠又能够与硫酸铜发生复分解反应,以此解答该题.
解答 解:A.钠投入溶液中,发生的反应实质是钠与酸或者水电离产生的氢离子的反应,钠与盐酸反应的实质为:2Na+2H+=2Na++H2↑,故A错误;
B.钠的密度比水小,可在液面的上方,故B正确;
C.钠与硫酸铜溶液反应,方程式为:2Na+2H2O=2NaOH+H2↑,2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,故C正确;
D.依据得失电子守恒,可知相同量的钠失去电子数相同,生成氢气的量相同,故D正确;
故选A.
点评 本题考查了钠的性质,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,难度不大,注意把握钠的性质,特别时钠与硫酸铜反应的特点,为易错点.

练习册系列答案
相关题目
14.常温下,下列说法错误的是( )
| A. | pH=6的NaHSO4溶液:c(Na+)+c(H+)=2c(SO42-)+c(OH-) | |
| B. | 0.1 mol/L NaHCO3溶液加水稀释后,c(H+)与c(OH-)的乘积不变 | |
| C. | pH相同的①CH3COONa、②NaClO二种溶液的c(Na+):①<② | |
| D. | 0.1 mol/L Na2SO3溶液:c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3) |
15.二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物形式完全沉淀时,溶液的pH及部分硫化物的Ksp(均为25℃时)见下表,.
回答下列问题:
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为2FeSO4+MnO2+2H2SO4=MnSO4+Fe2(SO4)3+2H2O
(2)滤渣B的主要成分是Fe(OH)3和Al(OH)3.
(3)加入MnS的目的是除去Cu2+,Zn2+杂质,可能原因是CuS、ZnS的溶解度较MnS小.
(4)碱性锌锰干电池在放电时,电池的总反应方程式可以表示为:Zn+2MnO2+2H2O═Zn(OH)2+2MnOOH,该电池的正极反应式为2MnO2+2H2O+2e-═2MnOOH+2OH-.

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物形式完全沉淀时,溶液的pH及部分硫化物的Ksp(均为25℃时)见下表,.
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 |
| 沉淀物 | CuS | ZnS | MnS | FeS | ||
| Ksp | 8.5×10-45 | 1.2×10-23 | 1.4×10-15 | 3.7×10-14 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为2FeSO4+MnO2+2H2SO4=MnSO4+Fe2(SO4)3+2H2O
(2)滤渣B的主要成分是Fe(OH)3和Al(OH)3.
(3)加入MnS的目的是除去Cu2+,Zn2+杂质,可能原因是CuS、ZnS的溶解度较MnS小.
(4)碱性锌锰干电池在放电时,电池的总反应方程式可以表示为:Zn+2MnO2+2H2O═Zn(OH)2+2MnOOH,该电池的正极反应式为2MnO2+2H2O+2e-═2MnOOH+2OH-.
10.如图为铜锌原电池的示意图,下列有关的说法中不正确的是( )
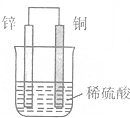

| A. | 锌片上有H2逸出 | B. | 溶液中c(H+)逐渐减小 | ||
| C. | 正极反应式:2H++2e-═H2↑ | D. | 负极反应式:Zn-2e-═Zn2+ |
17.有文献报道,硫在空气中燃烧时,产物中SO3约占5%~6%(体积比,下同),而硫在纯氧气中燃烧时,其产物中的SO3约占2%~3%,解释这一事实的理由正确的是( )
| A. | 在空气中燃烧时,硫的燃烧热小,使化学平衡向有利于生成SO3的方向移动 | |
| B. | 在纯氧气中燃烧时,硫的燃烧热大,不利于化学平衡向生成SO3的方向移动 | |
| C. | 在硫燃烧的过程中,对于SO3的生成,温度的影响大于氧气浓度的影响 | |
| D. | 没有使用催化剂 |
7.如图是电解MgCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断不正确的是( )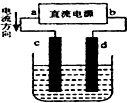

| A. | c、d电极上都有气体产生 | B. | d为阴极、c为阳极 | ||
| C. | d极附近溶液PH值升高 | D. | 电解过程中,氯离子浓度减小 |
14.比较是化学学习中的一种重要方法.下列各组比较中不正确的是( )
| A. | 在相同条件下的溶解度:NaHCO3>Na2CO3 | |
| B. | 还原性:I->Br->Cl->F- | |
| C. | 氧化性:F2>Cl2>Br2>I2 | |
| D. | 碳酸氢钠溶液与稀盐酸互滴时两种操作现象相同 |
11.下列实验设计和结论相符的是( )
| A. | 某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 | |
| B. | 向稀硝酸中加入铁粉完全反应,所得溶液一定只含一种溶质 | |
| C. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| D. | 在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净FeCl3溶液 |
12.下列说法正确的是( )
| A. | 任何情况下,温度都不可能对反应的方向起决定性作用 | |
| B. | pH=4的CH3COOH和NH4Cl溶液中,水的电离程度相同 | |
| C. | 用pH试纸测定溶液pH的正确操作是,将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照 | |
| D. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |