题目内容
1.铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是( )| A. | Fe(OH)3 Fe2O3 | B. | Fe(OH)2 Fe2O3 | C. | Fe(OH)2 Fe(OH)3 | D. | Fe(OH)2 Fe3O4 |
分析 铁屑溶于过量的稀硫酸,反应生成硫酸亚铁,过滤后向滤液中再加入过量的氨水,反应生成氢氧化亚铁沉淀,放置一段时间后,氢氧化亚铁被氧化成氢氧化铁沉淀,氢氧化铁不稳定分解生成三氧化二铁.
解答 解:铁屑溶于过量的稀硫酸,反应生成硫酸亚铁,硫酸亚铁与足量氨水反应生成氢氧化亚铁白色沉淀,在空气中氢氧化亚铁容易被空气中的氧气氧化成氢氧化铁,氢氧化铁为红褐色沉淀,受热分解生成红棕色三氧化二铁,
故选:B.
点评 本题考查铁及铁的化合物的性质,是高考的热门考点,掌握铁及其氢氧化物的化学性质是解答的关键,题目难度不大.

练习册系列答案
相关题目
11.有三种不同取代基-X,-Y,-Z,当它们同时取代苯分子中的3个氢原子,取代产物有( )
| A. | 4种 | B. | 6种 | C. | 10种 | D. | 14种 |
12.下列物质属于共价化合物的是( )
| A. | NH4Cl | B. | H2SO4 | C. | I2 | D. | NaCl |
16.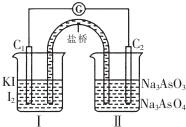 已知可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如图装置,进行下述操作:
已知可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如图装置,进行下述操作:
①向(Ⅱ)烧杯中逐滴加入浓盐酸,发现微安表(G)指针偏转;(提示:按正反应发生)
②若改往(Ⅱ)烧杯中滴加40%NaOH溶液,发现微安表指针与①的偏转方向相反.(提示:按逆反应发生)
下列有关说法中不正确的是( )
 已知可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如图装置,进行下述操作:
已知可逆反应AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如图装置,进行下述操作:①向(Ⅱ)烧杯中逐滴加入浓盐酸,发现微安表(G)指针偏转;(提示:按正反应发生)
②若改往(Ⅱ)烧杯中滴加40%NaOH溶液,发现微安表指针与①的偏转方向相反.(提示:按逆反应发生)
下列有关说法中不正确的是( )
| A. | ①操作过程中C1棒上发生的反应为2I--2e-═I2 | |
| B. | ②操作过程中盐桥中的阳离子移向(Ⅰ)烧杯 | |
| C. | 若将微安表换成惰性电极电解饱和食盐水的装置,在①操作过程中与C1棒连接的电极上有Cl2产生 | |
| D. | 若将微安表换成电解精炼铜装置,在②操作过程中与C2棒连接的为纯铜电极 |
6.下列说法正确的是( )
| A. | 按系统命名法,化合物 的名称为2,4-二乙基-6-丙基辛烷 的名称为2,4-二乙基-6-丙基辛烷 | |
| B. | 若两种二肽互为同分异构体,则二者的水解产物一定不相同 | |
| C. | 醋酸和硬脂酸互为同系物,C2H6和C9H20也一定互为同系物 | |
| D. | 某有机物的结构简式为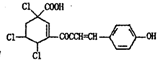 ,1mol该有机物通过消去反应脱去1 molHCl时,能得到5种不间产物(不考虑立体异构) ,1mol该有机物通过消去反应脱去1 molHCl时,能得到5种不间产物(不考虑立体异构) |
13.对于可逆反应C(s)+H2O(g)?CO+H2一Q.下列说法正确的是( )
| A. | 由于反应前后分子数相等,所以加压后,平衡不移动 | |
| B. | 平衡时c(H2O)(g)、c(CO)、c(H2)保持不变 | |
| C. | 达到平衡时,c(H2O)(g)═c(CO)=c(H2) | |
| D. | 升高温度,V正增大,V逆减小,所以平衡向右移动 |
10.下列说法错误的是( )
| A. | 0.1 mol•L-1的CH3COOH溶液中,由水电离的c(H+)为10-13 mol•L-1 | |
| B. | pH=2与pH=1的CH3COOH溶液中c(H+)之比为1:10 | |
| C. | 等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,混合后溶液pH<7 | |
| D. | 1 mol醋酸分子中含有共价键的个数为8NA |
11.在一定温度下,将100mL 氮气和氢气的混合气体充入等压密闭容器中进行反应,达平衡时维持温度不变,测得混合气体的密度是反应前密度的1.25倍,则达到平衡时,氨气的体积分数为( )
| A. | 25% | B. | 27.5% | C. | 30% | D. | 37.5% |
 将一定质量的镁铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入5mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.
将一定质量的镁铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入5mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.