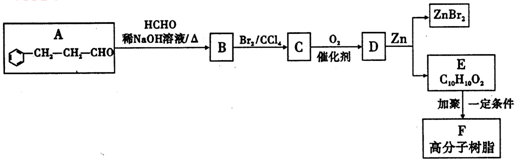
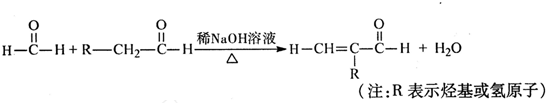
题目内容
下列物质中属于强电解质的是( )
| A、H2O |
| B、H2SO3 |
| C、铜 |
| D、NH4Cl |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液里全部电离的是强电解质,部分电离属于若电解质,电解质属于化合物,据此解答即可.
解答:
解:A.水部分电离,属于弱电解质,故A错误;
B.亚硫酸在水溶液中不能完全电离,亚硫酸是弱酸,属于弱电解质,故B错误;
C.金属铜是单质,它既不是电解质也不是非电解质,故C错误;
D.氯化铵属于盐,溶于水或者熔融状态时,可以完全电离变成氯离子和铵根离子,能导电,属于强电解质,故D正确;
故选D.
B.亚硫酸在水溶液中不能完全电离,亚硫酸是弱酸,属于弱电解质,故B错误;
C.金属铜是单质,它既不是电解质也不是非电解质,故C错误;
D.氯化铵属于盐,溶于水或者熔融状态时,可以完全电离变成氯离子和铵根离子,能导电,属于强电解质,故D正确;
故选D.
点评:本题考查了强弱电解质的判断,把握电解质的定义,分清强弱电解质的本质区别,注意单质既不是电解质也不是非电解质,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
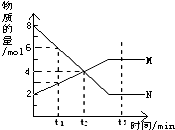 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:2N?M |
| B、Bt2时,正逆反应速率相等,达到平衡 |
| C、t1时,N的浓度是M的浓度的2倍 |
| D、t3时,正反应速率大于逆反应速率 |
常温下,下列电解质溶液的有关叙述正确的是( )
| A、新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| C、pH═11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| D、同浓度同体积的强酸与强碱溶液混合后,溶液的pH=7 |
25℃时,向含有AgCl(s)的饱和AgCl溶液中加水,下列叙述正确的是( )
| A、AgCl的溶解度增大 |
| B、AgCl的溶解度、Ksp均不变 |
| C、Ksp(AgCl)增大 |
| D、AgCl的溶解度、Ksp均增大 |
下列电解质溶液的有关叙述正确的是( )
| A、在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |
| B、pH=3的CH3COOH与pH=11的NaOH溶液等体积混合后,溶液显碱性 |
| C、将足量CuSO4溶液在0.1mol?L-1的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol?L-1(已知:Ksp(CuS)=1.3×10-36) |
| D、含1molKOH的溶液与1molCO2完全反应后,溶液中c(K+)=c(HCO3-) |
提供人体所需热能的最主要物质是( )
| A、蛋白质 | B、淀粉 | C、油脂 | D、水 |