题目内容
25℃时,向含有AgCl(s)的饱和AgCl溶液中加水,下列叙述正确的是( )
| A、AgCl的溶解度增大 |
| B、AgCl的溶解度、Ksp均不变 |
| C、Ksp(AgCl)增大 |
| D、AgCl的溶解度、Ksp均增大 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:一定温度下AgCl的溶解度、溶度积为定值,二者只受温度影响,据此结合选项解答.
解答:
解:A、加入水多,溶解的氯化银质量多,AgCl的溶解度是指一定温度下,100g水中溶解AgCl的最大质量,与加入水的多少无关,故A错误;
B、AgCl的溶解度、Ksp只受温度影响,温度不变,AgCl的溶解度、Ksp不变,故B正确;
C、AgCl的Ksp只受温度影响,温度不变,AgCl的Ksp不变,故C错误;
D、AgCl的溶解度、Ksp只受温度影响,温度不变,AgCl的溶解度、Ksp不变,故D错误;
故选B.
B、AgCl的溶解度、Ksp只受温度影响,温度不变,AgCl的溶解度、Ksp不变,故B正确;
C、AgCl的Ksp只受温度影响,温度不变,AgCl的Ksp不变,故C错误;
D、AgCl的溶解度、Ksp只受温度影响,温度不变,AgCl的溶解度、Ksp不变,故D错误;
故选B.
点评:本题考查溶解度、溶度积含义与影响因素等,难度不大,注意溶解度、溶度积只受温度影响.

练习册系列答案
相关题目
常温下,关于下列各溶液的叙述不正确的是( )
| A、pH=7的醋酸钠和醋酸的混合溶液中,c(Na+)=c(CH3COO-) |
| B、O.1mol?L-1的醋酸的pH=a,0.01mol?L-1的醋酸的pH=b,则a+1>b>a |
| C、20mL0.1mol?L-1醋酸钠溶液与10mL0.1mol?L-1盐酸混合后溶液显酸性,则c(H+)+c(Na+)=c(CH3COO-)+c(Cl-) |
| D、已知酸性:HF>CH3COOH,pH相等的NaF溶液与CH3COOK溶液中,[c(Na+)-c(F-)]<[c(K+)-c(CH3COO-)] |
电极电解某金属的氯化物(MCl2)溶液,当阳极上收集到1.12L Cl2时(标准状况),阴极增重3.2g.下列有关叙述正确的是( )
| A、M的相对原子质量为32 |
| B、电解过程中溶液的pH不发生变化 |
| C、M的相对原子质量为64 |
| D、电路中通过0.5mol电子 |
下列物质中属于强电解质的是( )
| A、H2O |
| B、H2SO3 |
| C、铜 |
| D、NH4Cl |
下列式子中,属于水解反应的是( )
| A、H2O+H2O?H3O++OH- |
| B、CO32-+H2O?HCO3-+OH- |
| C、NH3+H2O?NH3.H2O |
| D、HCO3-+OH-?H2O+CO32- |
已知25℃时有关弱电解质的电离平衡常数:
根据上述电离平衡常数分析,下列推断错误的是( )
| 弱电解质 | 醋酸 | 苯酚 | 碳酸 |
| 电离平衡常数(25℃) | 1.8×10-5 | 1.28×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、25℃时,等物质的量浓度的下列溶液pH关系为:pH(Na2CO3)>pH(C6H5ONa)>pH(NaHCO3)>pH(CH3COONa) |
| B、若amol/L苯酚与bmol/LNaOH两溶液等体积混合后,溶液中c(Na+)=c(C6H5O-),则a一定大于b |
| C、C6H5ONa溶液中通少量CO2气体:2C6H5ONa+H2O=CO2→2C6H5OH+Na2CO3 |
| D、足量的CH3COOH与Na2CO3溶液混合:2CH3COOH+Na2CO3═2CH3COONa+H2O+CO2↑ |
下列表述中正确的是( )
| A、任何能使熵值增大的过程都能自发进行 |
| B、已知热化学方程式2SO2(g)+O2(g)?2SO3(g)△H=-QkJ?mol-1(Q>0),则将2molSO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出QkJ的热量 |
| C、化学平衡发生移动,平衡常数一定发生变化 |
| D、足量的锌粒分别和等体积同浓度的CH3COOH、HCl反应,两者放出氢气质量相同 |
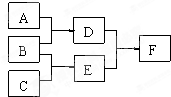 单质A、B、C和化合物D、E、F,在一定条件下有如下图的转化关系:(有部分反应物或者生成物未标出)
单质A、B、C和化合物D、E、F,在一定条件下有如下图的转化关系:(有部分反应物或者生成物未标出)