题目内容
10.若取等质量的铝粉分别与足量的稀盐酸和NaOH溶液反应,所得氢气的体积在同样条件下相比( )| A. | 与酸反应产生氢气多 | B. | 与碱反应产生氢气多 | ||
| C. | 一样多 | D. | 不知道铝粉的质量,无法比较 |
分析 Al和稀盐酸、NaOH溶液反应时都是Al作还原剂,根据Al和氢气之间的关系式分析解答.
解答 解:Al和稀盐酸、NaOH溶液反应时都是Al作还原剂,Al的质量相同则Al的物质的量相同,n(Al)相同则转移电子物质的量相同,所以在相同条件下生成氢气体积相同,故选C.
点评 本题考查氧化还原反应计算,侧重考查学生分析判断能力,明确氢气体积大小与Al的量有关而与酸碱的量无关是解本题关键,注意:如果是足量的Al分别与相同物质的量的稀盐酸和NaOH溶液反应时NaOH溶液生成的氢气多,题目难度不大.

练习册系列答案
相关题目
20.(1)用O2将HC1转化为Cl2,可提高效益,减少污染,传统上该转化通过如图所示的催化剂循环实现,

其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(s)△H1,反应②生成1mol Cl2 (g)的反应热为△H2,则总反应的热化学方程式为2HCl(g)+$\frac{1}{2}$O2(g)$\frac{\underline{\;\;△\;\;}}{\;}$H2O(g)+Cl2(g)△H=△H1+△H2.(反应热用△H1和△H2表示).
(2)一定条件下测得上述反应过程中c(Cl2)的数据如下:
计算2.0~6.0min内以HCl的物质的量浓度变化表示的反应速率1.8×10-3mol/(L•min).
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生.
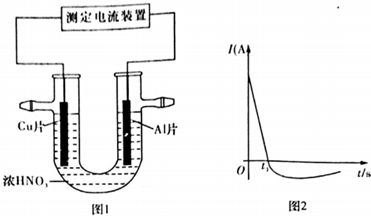
0~tl时,原电池的负极是Al片,此时,正极的电极反应式是2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动,tl时,原电池中电子流动方向发生改变,其原因是铝钝化后,铜成为负极.

其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(s)△H1,反应②生成1mol Cl2 (g)的反应热为△H2,则总反应的热化学方程式为2HCl(g)+$\frac{1}{2}$O2(g)$\frac{\underline{\;\;△\;\;}}{\;}$H2O(g)+Cl2(g)△H=△H1+△H2.(反应热用△H1和△H2表示).
(2)一定条件下测得上述反应过程中c(Cl2)的数据如下:
| t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| N(Cl2)/10-3(mol/L) | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生.

0~tl时,原电池的负极是Al片,此时,正极的电极反应式是2H++NO3-+e-=NO2↑+H2O,溶液中的H+向正极移动,tl时,原电池中电子流动方向发生改变,其原因是铝钝化后,铜成为负极.
18.下列有关氨或铵盐的说法不正确的是( )
| A. | NH3属于弱电解质 | |
| B. | 可用湿润的红色石蕊试纸检验氨气 | |
| C. | 用盐酸滴定氨水,当溶液呈中性时,c(NH4+)=c(Cl-) | |
| D. | 常温时,0.1mol•L-1NH4Cl溶液加水稀释,$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)•c({H}^{+})}$的值不变 |
5.为除去某物质中所含的杂质,所选用的试剂或操作方法正确的是( )
| 序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
| ① | NaCl溶液 | Na2CO3 | 加入盐酸,蒸发 |
| ② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
| ③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| ④ | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
| A. | ①②③④ | B. | ②③④ | C. | ①③④ | D. | ①②③ |
2. 某实验小组对一含有Al3+的未知溶液进行分析:往该溶液逐滴滴加某浓度NaOH溶液,所加NaOH溶液体积(ml)与产生沉淀的物质的量(mol)的关系如下图所示:下列说法错误的是( )
某实验小组对一含有Al3+的未知溶液进行分析:往该溶液逐滴滴加某浓度NaOH溶液,所加NaOH溶液体积(ml)与产生沉淀的物质的量(mol)的关系如下图所示:下列说法错误的是( )
 某实验小组对一含有Al3+的未知溶液进行分析:往该溶液逐滴滴加某浓度NaOH溶液,所加NaOH溶液体积(ml)与产生沉淀的物质的量(mol)的关系如下图所示:下列说法错误的是( )
某实验小组对一含有Al3+的未知溶液进行分析:往该溶液逐滴滴加某浓度NaOH溶液,所加NaOH溶液体积(ml)与产生沉淀的物质的量(mol)的关系如下图所示:下列说法错误的是( )| A. | 该未知溶液中至少含有3种阳离子 | |
| B. | 滴加的NaOH溶液的物质的量浓度为5mol•L-1 | |
| C. | 若将最终沉淀过滤、洗涤、灼烧,其质量一定为6 g | |
| D. | 若溶液中仅有两种金属阳离子,且另一种离子为二价阳离子,则a=10 |
19.在密闭容器中发生可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),以下是不同情况下的反应速率,其中最快的是( )
| A. | v(O2)=0.01 mol•L-1•s-1 | B. | v(NH3)=0.02mol•L-1•s-1 | ||
| C. | v(H2O)=0.06 mol•L-1•min-1 | D. | v(NO)=0.03mol•L-1•s-1 |