题目内容
下列实验操作正确的是( )
| A、在2mL10%的氢氧化钠溶液中滴入2%的硫酸铜溶液4~6滴,配制新制氢氧化铜悬浊液,检验醛基 |
| B、实验室制乙烯时,迅速升温到140℃ |
| C、用乙醇和浓硫酸除去乙酸乙酯中混有的少量乙酸 |
| D、用苯、2mol/L的硝酸和3mol/L的硫酸制硝基苯 |
考点:化学实验方案的评价,乙烯的实验室制法,苯的性质,物质的分离、提纯和除杂
专题:实验评价题,有机物的化学性质及推断
分析:A.2mL10%的氢氧化钠溶液中滴入2%的硫酸铜溶液4~6滴,碱过量,碱性条件可检验醛基;
B.制乙烯时,利用乙醇和浓硫酸加热只170℃;
C.乙醇易溶于乙酸乙酯,且酯化反应为可逆反应;
D.2mol/L的硝酸和3mol/L的硫酸均不是浓酸.
B.制乙烯时,利用乙醇和浓硫酸加热只170℃;
C.乙醇易溶于乙酸乙酯,且酯化反应为可逆反应;
D.2mol/L的硝酸和3mol/L的硫酸均不是浓酸.
解答:
解:A.2mL10%的氢氧化钠溶液中滴入2%的硫酸铜溶液4~6滴,碱过量,则配制新制氢氧化铜悬浊液与含-CHO的物质生成砖红色沉淀可检验醛基,故A正确;
B.制乙烯时,利用乙醇和浓硫酸加热只170℃,而140℃时生成乙醚,故B错误;
C.乙醇易溶于乙酸乙酯,且酯化反应为可逆反应,不能除杂,应利用饱和碳酸钠溶液除去乙酸乙酯中混有的少量乙酸,故C错误;
D.2mol/L的硝酸和3mol/L的硫酸均不是浓酸,应利用苯、浓硝酸、浓硫酸制备硝基苯,故D错误;
故选A.
B.制乙烯时,利用乙醇和浓硫酸加热只170℃,而140℃时生成乙醚,故B错误;
C.乙醇易溶于乙酸乙酯,且酯化反应为可逆反应,不能除杂,应利用饱和碳酸钠溶液除去乙酸乙酯中混有的少量乙酸,故C错误;
D.2mol/L的硝酸和3mol/L的硫酸均不是浓酸,应利用苯、浓硝酸、浓硫酸制备硝基苯,故D错误;
故选A.
点评:本题考查化学实验方案的评价,为高频考点,涉及醛基的检验、乙烯的制备、硝基苯的制备及物质的除杂等,把握物质的性质及化学反应原理为解答的关键,注意实验的评价性分析,题目难度不大.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
下列有关化学用语表示正确的是( )
A、CaH2的电子式: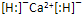 | ||
B、Cl-的结构示意图: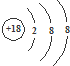 | ||
C、质子数为92、中子数为146的U原子:
| ||
D、CH2F2的电子式: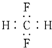 |
下列化学反应中,离子方程式表示正确的是( )
| A、用小苏打(NaHCO3)治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| B、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、往氢氧化钠中滴加氯化铜溶液:Cu2++2OH-=Cu(OH)2↓ |
| D、铜片插入硝酸银溶液:Cu+Ag+═Cu2++Ag |
下列说法中,正确的是( )
| A、SiO2是硅酸的酸酐,可与水化合生成硅酸 |
| B、CO2通入水玻璃中可以得到硅酸 |
| C、在高温是SiO2与Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 |
| D、SiO2是酸性氧化物,它不溶于任何酸 |
下列关于物质的量、摩尔质量的叙述正确的是( )
| A、0.012 kg 12C中含有约6.02×1023个碳原子 |
| B、1 mol H2O中含有2 mol氢和1 mol氧 |
| C、氢氧化钠的摩尔质量是40 g |
| D、2 mol水的摩尔质量是1 mol水的摩尔质量的2倍 |
 在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)═2HBr(g)△H<0.当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是( )
在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)═2HBr(g)△H<0.当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是( )| A、若b、c点的平衡常数分别为K1、K2,则K1>K2 |
| B、a、b两点的反应速率:b>a |
| C、为了提高Br2(g)的转化率,可采取增加Br2(g)通入量的方法 |
| D、若平衡后保持温度不变,压缩容器体积平衡一定不移动 |
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、5.6g Fe与足量稀盐酸反应转移的电子数为0.3NA |
| B、常温常压下,23g NO2含有NA个氧原子 |
| C、标准状况下,22.4L水含有个NA H2O分子 |
| D、1mol/L NaCl溶液含有NA个Na+ |
 →
→