题目内容
下列有关化学用语表示正确的是( )
A、CaH2的电子式: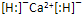 | ||
B、Cl-的结构示意图: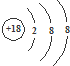 | ||
C、质子数为92、中子数为146的U原子:
| ||
D、CH2F2的电子式: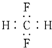 |
考点:电子式,常见元素的名称、符号、离子符号,原子结构示意图
专题:化学用语专题
分析:A.CaH2的是由2个[H-]与Ca2+通过离子键结合形成的离子化合物;
B.Cl为17号元素,核内有17个质子;
C.元素符号左上角数字表示质量数,质量数=质子数+中子数;
D.F原子为成键的孤对电子对未画出.
B.Cl为17号元素,核内有17个质子;
C.元素符号左上角数字表示质量数,质量数=质子数+中子数;
D.F原子为成键的孤对电子对未画出.
解答:
解:A.CaH2的是由2个[H-]与Ca2+通过离子键结合形成的离子化合物,CaH2的电子式为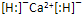 ,故A正确;
,故A正确;
B.Cl为17号元素,核内有17个质子,Cl-的结构示意图为 ,故B错误;
,故B错误;
C.质子数为92、中子数为146,则质量数为238,U原子表示为92238U,故C错误;
D.CH2F2的电子式为 ,故D错误;
,故D错误;
故选:A.
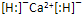 ,故A正确;
,故A正确;B.Cl为17号元素,核内有17个质子,Cl-的结构示意图为
 ,故B错误;
,故B错误;C.质子数为92、中子数为146,则质量数为238,U原子表示为92238U,故C错误;
D.CH2F2的电子式为
 ,故D错误;
,故D错误;故选:A.
点评:本题考查常用化学用语的书写,难度中等,D选项为易错点,容易忽略未成键的孤对电子对.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
下列说法正确的是( )
| A、可用丁达尔效应区分溶液与胶体 |
| B、NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质 |
| C、配制硫酸溶液时,先在量筒中加入一定量的水,再慢慢加入浓硫酸 |
| D、浓碱溶液溅到皮肤上,要立即用大量水冲洗,然后抹上碳酸钠溶液 |
可逆反应3H2+N2?2NH3达到平衡的标志是( )
①消耗3mol H2的同时生成2mol NH3
②1个N≡N键断裂的同时,有3个H-H键形成
③H2、N2与NH3的物质的量之比为3:1:2
④1个N≡N键断裂的同时,有6个N-H键断裂
⑤1个N≡N键断裂的同时,有6个N-H键形成.
①消耗3mol H2的同时生成2mol NH3
②1个N≡N键断裂的同时,有3个H-H键形成
③H2、N2与NH3的物质的量之比为3:1:2
④1个N≡N键断裂的同时,有6个N-H键断裂
⑤1个N≡N键断裂的同时,有6个N-H键形成.
| A、①②⑤ | B、②④ |
| C、①②③④ | D、全部 |
运用元素周期律分析下面的推断,其中不正确的是( )
| A、酸性:HClO4>HBrO4>HIO4 |
| B、砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 |
| C、在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 |
| D、稳定性:PH3>H2S>HCl |
下列溶液中的Cl-浓度与100mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )
| A、150 mL 1mol/LNaCl溶液 |
| B、75mL 1mol/L CaCl2溶液 |
| C、150 mL 0.2mol/LKCl溶液 |
| D、75mL 1mol/LAlCl3溶液 |
下列各组离子可能在指定溶液中大量共存的是( )
| A、pH=11的溶液中:Na+,AlO2-,S2-,SO32- |
| B、加入Al能放出H2的溶液中:Mg2+,NO3-,K+,SO42- |
| C、使石蕊变红的溶液中:Cu2+,Cl-,Na+,SO42- |
| D、水电离的H+浓度c(H+)=10-12mol/L的溶液中:Cl-,HCO3-,NO3-,S2O32- |
下列物质分别与CuSO4、NaCl、Fe2(SO4)3、MgSO4等溶液混合时,产生的现象各不相同的是( )
| A、盐酸 | B、氢氧化钾溶液 |
| C、氯化钡溶液 | D、硫酸钠溶液 |
白酒、食醋、蔗糖、淀粉是家庭厨房中常用的烹调剂,利用这些物质能完成的实验是( )
| A、鉴别食盐和小苏打 |
| B、检验食盐中是否含KIO3 |
| C、检验自来水中是否含有氯离子 |
| D、检验白酒中是否含甲醇 |
下列实验操作正确的是( )
| A、在2mL10%的氢氧化钠溶液中滴入2%的硫酸铜溶液4~6滴,配制新制氢氧化铜悬浊液,检验醛基 |
| B、实验室制乙烯时,迅速升温到140℃ |
| C、用乙醇和浓硫酸除去乙酸乙酯中混有的少量乙酸 |
| D、用苯、2mol/L的硝酸和3mol/L的硫酸制硝基苯 |