题目内容
向AgCl饱和溶液中滴加足量NaBr溶液,产生淡黄色沉淀,再向溶液中滴加KI溶液又产生黄色沉淀.有关下列说法正确的是( )
| A、产生的淡黄色沉淀为AgI |
| B、产生的黄色沉淀为AgBr |
| C、由上述实验现象可说明溶解度S(AgBr)>S(AgI)>S(AgCl) |
| D、上述实验理解说明沉淀可相互转化 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:向AgCl饱和溶液中滴加足量NaBr溶液,产生淡黄色沉淀为AgBr,再向溶液中滴加KI溶液又产生黄色沉淀为AgI,依据反应现象可知实现程度转化的依据是向更难溶的物质进行;
解答:
解:向AgCl饱和溶液中滴加足量NaBr溶液,产生淡黄色沉淀为AgBr,再向溶液中滴加KI溶液又产生黄色沉淀为AgI,是沉淀转化原理的应用,溶解度大小,氯化银>溴化银>碘化银;
A、产生的淡黄色沉淀为AgBr,故A错误;
B、产生的黄色沉淀为AgI,故B错误;
C、由上述实验现象可说明溶解度S(AgI)<S(AgBr)<S(AgCl),故C错误;
D、向AgCl饱和溶液中滴加足量NaBr溶液,产生淡黄色沉淀为AgBr,再向溶液中滴加KI溶液又产生黄色沉淀为AgI,上述实验理解说明沉淀可相互转化,故D正确;
故选D.
A、产生的淡黄色沉淀为AgBr,故A错误;
B、产生的黄色沉淀为AgI,故B错误;
C、由上述实验现象可说明溶解度S(AgI)<S(AgBr)<S(AgCl),故C错误;
D、向AgCl饱和溶液中滴加足量NaBr溶液,产生淡黄色沉淀为AgBr,再向溶液中滴加KI溶液又产生黄色沉淀为AgI,上述实验理解说明沉淀可相互转化,故D正确;
故选D.
点评:本题考查了沉淀溶解平衡的分析应用,主要是沉淀转化的原理分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列正确的是( )
| A、将一定量氨气通入0.1 mol?L-1 NH4Cl溶液中可能有:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、AgCl沉淀易转化成AgI沉淀且Ksp(AgX)=c(Ag+)?c(X-),故Ksp(AgI)>K(AgCl) |
| C、F、Cl、Br、I的非金属性逐渐减弱,HF、HCl、HBr、HI水溶液的酸性逐渐减弱 |
| D、短周期元素形成离子后,最外层均达8电子稳定结构 |
对于难溶盐MX,其饱和溶液中M+和X-的物质的量浓度之间存在关系等式Ksp=c(M+)?c(X-).现将足量的AgCl分别放入下列物质中,AgCl的溶解度最大的是( )
| A、40 mL 0.03 mol?L-1HCl溶液 |
| B、20 mL 0.02 mol?L-1KCl溶液 |
| C、30 mL 0.02 mol?L-1CaCl2溶液 |
| D、50 mL 0.05 mol?L-1AgNO3溶液 |
在AgCl沉淀中加过量KI溶液,白色沉淀转化为黄色沉淀,有关结论不正确的是( )
| A、加过量KI溶液充分反应后,Ksp(AgCl)减小 |
| B、加过量KI溶液充分反应后,溶液中Ag+和I-的浓度之积等于Ksp(AgI) |
| C、加过量KI溶液充分反应后,溶液中Ag+和Cl-的浓度之积小于Ksp(AgCl) |
| D、Ksp(AgI)<Ksp(AgCl) |
有关AgCl的沉淀溶解平衡的说法中,不正确的是( )
| A、在盐酸溶液中,AgCl的溶解度会减小 |
| B、向存在AgCl沉淀的少量溶液中加入NaI固体,会生成黄色沉淀 |
| C、向AgNO3溶液中加入足量盐酸,反应后的溶液中没有Ag+ |
| D、达到沉淀溶解平衡时,AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
在测定中和热的实验中,使用下列用品不是为了减小实验误差的是( )
| A、碎泡沫塑料 | B、环形玻璃棒 |
| C、硬纸板 | D、两个量筒 |
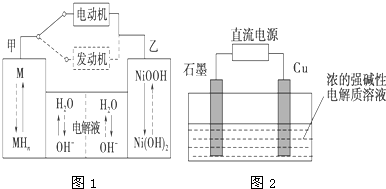 运用相关原理,回答下列问题:
运用相关原理,回答下列问题: