题目内容
在AgCl沉淀中加过量KI溶液,白色沉淀转化为黄色沉淀,有关结论不正确的是( )
| A、加过量KI溶液充分反应后,Ksp(AgCl)减小 |
| B、加过量KI溶液充分反应后,溶液中Ag+和I-的浓度之积等于Ksp(AgI) |
| C、加过量KI溶液充分反应后,溶液中Ag+和Cl-的浓度之积小于Ksp(AgCl) |
| D、Ksp(AgI)<Ksp(AgCl) |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:氯化银的溶解性大于碘化银,向AgCl饱和溶液中加入KI溶液,碘离子和银离子会结合为更难溶的碘化银沉淀.
解答:
解:AgCl饱和溶液中存在溶解沉淀平衡,AgCl(s)?Ag++Cl-,向AgCl饱和溶液中加入KI溶液,现象为白色沉淀转化为黄色沉淀,原因是氯化银的溶解性大于碘化银,碘离子会和银离子结合为更难溶的碘,
A、Ksp(AgCl)只与温度有关,故A错误;
B、AgI的饱和溶液中Ag+和I-的浓度之积等于Ksp(AgI),故B正确;
C、AgI的饱和溶液中Ag+和Cl-的浓度之积等于Ksp(AgI),故C正确;
D、氯化银的溶解性大于碘化银,故Ksp(AgI)<Ksp(AgCl),故D正确,
故选A.
A、Ksp(AgCl)只与温度有关,故A错误;
B、AgI的饱和溶液中Ag+和I-的浓度之积等于Ksp(AgI),故B正确;
C、AgI的饱和溶液中Ag+和Cl-的浓度之积等于Ksp(AgI),故C正确;
D、氯化银的溶解性大于碘化银,故Ksp(AgI)<Ksp(AgCl),故D正确,
故选A.
点评:本题考查了沉淀溶解平衡的分析判断,注意溶度积常数是温度的函数,沉淀可以实现沉淀转化,题目难度中等.

练习册系列答案
相关题目
常温,向一定体积V mL浓度均为 0.1mol?L-1 FeCl3和FeCl2溶液中滴加NaOH溶液至pH=4,溶液中有沉淀生成,过滤,得到沉淀和滤液.已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)2]=8.0×10-16.下列说法正确的是( )
| A、滤液中c(Fe3+)=4.0×10-29mol?L-1 |
| B、沉淀为Fe(OH)3和Fe(OH)2的混合物 |
| C、向滤液中加入少量FeCl2溶液,一定有沉淀生成 |
| D、向滤液中继续加入NaOH溶液使pH>7时,有Fe(OH)2沉淀生成 |
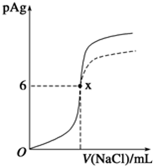 已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图是向10mL AgNO3溶液中逐渐加入0.1mol?L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )
已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图是向10mL AgNO3溶液中逐渐加入0.1mol?L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )| A、原AgNO3溶液的物质的量浓度为1mol?L-1 |
| B、图中x点的坐标为(100,6) |
| C、若升高温度,图象不会发生变化 |
| D、把0.1mol?L-1的NaCl换成0.1mol?L-1 NaI则图象在终点后变为虚线部分 |
已知Ksp(Ag2CrO4)=9.0×10-12,将等体积的4×10-3mol?L-1的AgNO3溶液和4×10-3mol?L-1的K2CrO4溶液混合,下列说法正确的是( )
| A、恰好形成Ag2CrO4饱和溶液 |
| B、能析出Ag2CrO4沉淀 |
| C、不能析出Ag2CrO4沉淀 |
| D、无法确定能否析出Ag2CrO4沉淀 |
向AgCl饱和溶液中滴加足量NaBr溶液,产生淡黄色沉淀,再向溶液中滴加KI溶液又产生黄色沉淀.有关下列说法正确的是( )
| A、产生的淡黄色沉淀为AgI |
| B、产生的黄色沉淀为AgBr |
| C、由上述实验现象可说明溶解度S(AgBr)>S(AgI)>S(AgCl) |
| D、上述实验理解说明沉淀可相互转化 |
下列说法正确的是( )
| A、海南岛四面环海,水资源丰富,不必节约用水 |
| B、明矾既能沉降水中的悬浮物,又能杀菌消毒 |
| C、可通过长期饮用含Ca2+浓度较高的水来补钙 |
| D、若不慎接触敌敌畏或甲胺磷,最好用碱性肥皂液清洗 |
如图所示的实验操作中正确的是( )
A、 二氧化碳的验满 |
B、 稀释浓硫酸 |
C、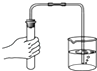 检查气密性 |
D、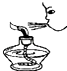 熄灭酒精灯 |