题目内容
有关AgCl的沉淀溶解平衡的说法中,不正确的是( )
| A、在盐酸溶液中,AgCl的溶解度会减小 |
| B、向存在AgCl沉淀的少量溶液中加入NaI固体,会生成黄色沉淀 |
| C、向AgNO3溶液中加入足量盐酸,反应后的溶液中没有Ag+ |
| D、达到沉淀溶解平衡时,AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A、依据AgCl的溶度积是个常数,取决于银离子浓度与氯离子浓度的成积,据此解答;
B、依据难溶物有向更难溶物转化的趋势解答;
C、氯化银难溶于水,但在水中存在沉淀溶解平衡,能溶解的全部电离;
D、沉淀溶解平衡时生成沉淀的速率和沉淀溶解的速率相同,是动态平衡.
B、依据难溶物有向更难溶物转化的趋势解答;
C、氯化银难溶于水,但在水中存在沉淀溶解平衡,能溶解的全部电离;
D、沉淀溶解平衡时生成沉淀的速率和沉淀溶解的速率相同,是动态平衡.
解答:
解:A、AgCl的溶度积是个常数,故银离子浓度与氯离子浓度成反比例关系,氯离子浓度增大,故银离子浓度减小,即AgCl的溶解度减小,故A正确;
B、AgI比AgCl更难溶于水,故向存在AgCl沉淀的少量溶液中加入NaI固体,会生成黄色沉淀,故B正确;
C、氯化银难溶于水,但在水中存在沉淀溶解平衡,能溶解的全部电离,溶液中有Ag+和Cl-,故C错误;
D、达到沉淀溶解平衡时,AgCl沉淀生成和沉淀溶解不断进行,是动态平衡,速率相等,故D正确,
故选C.
B、AgI比AgCl更难溶于水,故向存在AgCl沉淀的少量溶液中加入NaI固体,会生成黄色沉淀,故B正确;
C、氯化银难溶于水,但在水中存在沉淀溶解平衡,能溶解的全部电离,溶液中有Ag+和Cl-,故C错误;
D、达到沉淀溶解平衡时,AgCl沉淀生成和沉淀溶解不断进行,是动态平衡,速率相等,故D正确,
故选C.
点评:本题考查了沉淀溶解平衡的影响因素和平衡移动方向,物质溶解度的变化应用,题目较简单.

练习册系列答案
相关题目
向AgCl饱和溶液中滴加足量NaBr溶液,产生淡黄色沉淀,再向溶液中滴加KI溶液又产生黄色沉淀.有关下列说法正确的是( )
| A、产生的淡黄色沉淀为AgI |
| B、产生的黄色沉淀为AgBr |
| C、由上述实验现象可说明溶解度S(AgBr)>S(AgI)>S(AgCl) |
| D、上述实验理解说明沉淀可相互转化 |
已知:2A(s)+C2(g)=2AC(s)△H=-500kJ?mol-1;2B(l)+C2(g)=2BC(s)△H=-200kJ?mol-1
则反应A(s)+BC(s)=AC(s)+B(l)的△H为( )
则反应A(s)+BC(s)=AC(s)+B(l)的△H为( )
| A、+300 kJ?mol_1 |
| B、+150 kJ?mol_1 |
| C、-300 kJ?mol_1 |
| D、-150 kJ?mol_1 |
下列有关试剂的保存方法,错误的是( )
| A、金属钠保存在煤油中 |
| B、存放FeSO4溶液时加入少量铁粉 |
| C、NaOH溶液保存在带橡胶塞的玻璃试剂瓶中 |
| D、FeCl3溶液保存在广口瓶中 |
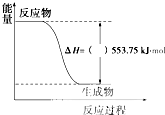 (1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:
(1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:

 800℃时,在2L密闭容器中发生2NO(g)+O2(g)?2NO2(g),测得n(NO)随时间的变化如下表:
800℃时,在2L密闭容器中发生2NO(g)+O2(g)?2NO2(g),测得n(NO)随时间的变化如下表: