题目内容
12.下列关于原子结构模型的演变顺序,按照先后顺序排列正确的是( )①卢瑟福的“带核原子模型”
②汤姆生的“葡萄干面包式”
③道尔顿的原子学说
④玻尔的原子结构模型(轨道理论)
| A. | ①③②④ | B. | ③②①④ | C. | ③①②④ | D. | ④③②① |
分析 ①1911年,卢瑟福的“带核原子模型”
②1904年,汤姆生的“葡萄干面包式”
③1808年,道尔顿的原子学说
④1913年,玻尔的原子结构模型(轨道理论).
解答 解:1808年,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体.
1897年,英国科学家汤姆生发现了电子,1904年提出“葡萄干面包式”的原子结构模型.
1911年英国物理学家卢瑟福(汤姆生的学生)提出了带核的原子结构模型.
1913年丹麦物理学家波尔(卢瑟福的学生)引入量子论观点,提出电子在一定轨道上运动的原子结构模型.
奥地利物理学家薛定谔提出电子云模型(几率说),为近代量子力学原子模型.
故原子结构模型的演变的过程为:道尔顿原子模型→汤姆生原子模型→卢瑟福原子模型→玻尔原子模型→量子力学模型,
故选B.
点评 本题考查了原子的结构和化学史,明确原子结构模型的演变的过程是关键,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
2.下表是Fe2+、Fe3+、Zn2+被OH-完全沉淀时溶液的pH.某硫酸锌酸性溶液中含有少量Fe2+、Fe3+杂质,为制得纯净的ZnSO4,应加入的试剂是( )
| 金属离子 | Fe2+ | Fe3+ | Zn2+ |
| 完全沉淀时的pH | 7.7 | 4.5 | 6.5 |
| A. | H2O2、ZnO | B. | 氨水 | C. | KMnO4、ZnCO3 | D. | NaOH溶液 |
20.某铁的“氧化物”样品,用5mol/L的盐酸140mL恰好完全溶解,所得溶液还能吸收标准状况下0.56L氯气,使其中Fe2+全部转化为Fe3+.该样品可能的化学式是( )
| A. | Fe2O3 | B. | Fe3O4 | C. | Fe4O5 | D. | Fe5O7 |
7.下列离子方程式书写正确的是( )
| A. | 烧碱溶液与小苏打溶液反应:OH-+HCO3-═H2O+CO2↑ | |
| B. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++H2O+CO2 | |
| C. | 氯化铝与过量氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | 硫酸氢钠与氢氧化钡1:1反应:SO42-+H++Ba2++OH-═BaSO4↓+H2O |
17.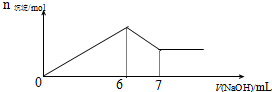 现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
 现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L 的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )| A. | 2:1 | B. | 2:3 | C. | 6:1 | D. | 3:1 |
4.取一小块金属钠放在燃烧匙中加热,下列实验现象描述正确的是( )
①金属钠先熔化 ②在空气中燃烧,产生黄色火焰 ③燃烧后得白色固体 ④燃烧后生成淡黄色固体物质.
①金属钠先熔化 ②在空气中燃烧,产生黄色火焰 ③燃烧后得白色固体 ④燃烧后生成淡黄色固体物质.
| A. | ①②④ | B. | ①②③ | C. | ①② | D. | ①②③④ |
1.今年以来,我国“高铁出口”成为新闻高频词,高铁产业的发展也给铝工业带来了春天.最近,美国密歇根州立大学国立超导回旋加速器实验室发现了超重铝42Al,关于42Al的说法错误的是( )
| A. | 属于金属元素 | B. | 中子数与质子数之差为29 | ||
| C. | 原子的核外电子数为13 | D. | 27Al和42Al是两种不同的核素 |
 .
.