题目内容
3.下列物质的类别与所含能团都正确的是( )(1)
 酚类-OH
酚类-OH(2)
 羧酸-COOH--
羧酸-COOH--(3)
 醛类
醛类
(4)CH3-O-CH3醚类

(5
 酯类
酯类
| A. | (1)(2)(3)(4)(5) | B. | (2)(4) | C. | (2)(3)(4) | D. | (2)(4)(5) |
分析 (1)羟基与苯环侧链的碳原子相连,该有机物为醇类;
(2)有机物分子中含有羧基,属于羧酸类物质;
(3)醛类的官能团是醛基;
(4)醚类物质含有 ;
;
(5)酯类物质的官能团为酯基.
解答 解:(1)该有机物分子中羟基没有与苯环直接相连,该有机物为醇类,不属于酚类,故错误;
(2)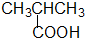 分子中含有羧基,属于羧酸类物质,故正确;
分子中含有羧基,属于羧酸类物质,故正确;
(3) 醛含有酯基,为酯,故错误;
醛含有酯基,为酯,故错误;
(4)CH3-O-CH3中 为醚键,属于醚类,故正确;
为醚键,属于醚类,故正确;
(5 含有醛基,为醛类,故错误;
含有醛基,为醛类,故错误;
故选B.
点评 本题考查了烃的衍生物的官能团、有机物的分类,题目难度不大,注意掌握烃的衍生物的官能团类型、有机物的分类方法,明确有机物分类方法与官能团类型的关系.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目
13.通常人体胃液的pH大约是0.9-1.5.胃液的酸碱性为( )
| A. | 碱性 | B. | 酸性 | C. | 无法判定 | D. | 中性 |
14.人们通常把拆开1mol某物质的化学键所吸收的能量看作该物质的化学键的键能,键能的大小可以衡量化学键的相对强弱.由图判断,下列说法错误的是( )


| A. | N≡N键的键能为946kJ•mol-1 | |
| B. | N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1 | |
| C. | 当有16gO2(g)参加反应时,该反应吸收90kJ热量 | |
| D. | 当有1mol电子发生转移时,该反应吸收90kJ热量 |
11.如图为元素周期表中短周期元素的一部分,下列关于Y、Z、M的说法正确的是( )
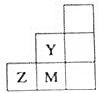

| A. | 非金属性:Y>Z>M | |
| B. | 离子半径:M->Z2->Y- | |
| C. | Z元素存在同素异形现象 | |
| D. | 三种元素中,Y的最高价氧化物对应的水化物酸性最强 |
18.下列有关叙述正确的是( )
| A. | Cl2、SO2均能使品红溶液褪色,说明二者均有漂白性 | |
| B. | 元素周期表中第IA族全部是金属元素 | |
| C. | 盛有浓硫酸的烧杯敞口放置一段时间后,质量增加 | |
| D. | 硫在纯氧中的燃烧产物是三氧化硫 |
15.下列物质的电子式错误的是( )
| A. | 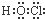 | B. | 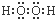 | C. | 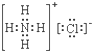 | D. | 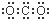 |
12.四种短周期主族元素在周期表中的相对位置如图所示,下列说法不正确的是( )
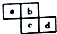

| A. | 原子半径:c>d>a>b | |
| B. | 原子序数d可能是a的3倍 | |
| C. | 最高价含氧酸的酸性c可能比d强 | |
| D. | 四种元素的氢化物可能是18电子分子 |
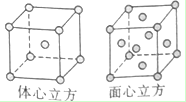 X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍.请回答下列问题:
X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍.请回答下列问题: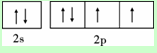 ,其第一电离能在同周期元素中由大到小排第4 位.
,其第一电离能在同周期元素中由大到小排第4 位.