题目内容
8. X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍.请回答下列问题:
X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,Y元素基态原子核外未成对电子数为2且X与Y形成的化合物在常温下为常见的液体R,Z元素原子最外电子层上s、p电子数相等,W基态原子3d轨道的电子数是4s轨道电子数的3倍.请回答下列问题:(1)Y基态原子的价电子排布图为
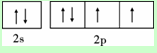 ,其第一电离能在同周期元素中由大到小排第4 位.
,其第一电离能在同周期元素中由大到小排第4 位.(2)W的元素名称为铁,其基态原子核外有26种空间运动状态不同的电子.
(3)R的中心原子采取的杂化方式为sp3,写出R的一个等电子体:H2S(或NH2-)(填化学式).
(4)Z与Y在一定条件下可形成高硬度的化合物,该化合物的晶体类型为原子晶体,其由Z、Y构成的最小环为12元环.
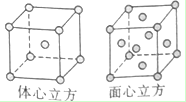
(5)W的单质在900℃以下为α型体心立方晶胞,910℃以上W转变为γ型面心立方晶胞,晶胞结构分别如图所示.两种晶体中距离最近的铁原子间距离相同.则在800℃和1000℃下,铁的密度之比为3$\root{3}{6}$:8.
分析 X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,则X为H元素,Y元素基态原子核外未成对电子数为2,且X与Y形成的化合物在常温下为常见的液体R,则Y为O元素,R为H2O,Z元素原子最外电子层上s、p电子数相等,且Z的原子序数大于氧,所以Z为Si元素,W基态原子3d轨道的电子数是4s轨道电子数的3倍,则W的外围电子排布为3d64s2,所以W为Fe元素,据此答题;
解答 解:X、Y、Z、W为前四周期元素且原子序数依次增大,X的电子层数等于核外电子数,则X为H元素,Y元素基态原子核外未成对电子数为2,且X与Y形成的化合物在常温下为常见的液体R,则Y为O元素,R为H2O,Z元素原子最外电子层上s、p电子数相等,且Z的原子序数大于氧,所以Z为Si元素,W基态原子3d轨道的电子数是4s轨道电子数的3倍,则W的外围电子排布为3d64s2,所以W为Fe元素,
(1)Y为O元素,价电子数为6,所以Y基态原子的价电子排布图为  ,其第一电离能在同周期元素中小于N、F、Ne,所以由大到小排第4位,
,其第一电离能在同周期元素中小于N、F、Ne,所以由大到小排第4位,
故答案为: ;4;
;4;
(2)W为Fe元素,W的元素名称为铁,其基态原子核外有26个电子,所以有26种空间运动状态不同的电子,
故答案:铁;26;
(3)R为H2O,R的中心原子价层电子对数为$\frac{6+2}{2}$=4,所以采取的杂化方式为sp3杂化,水的一个等电子体为H2S(或NH2-),
故答案为:sp3;H2S(或NH2-);
(4)Z为Si元素,Y为O元素,Z与Y在一定条件下可形成高硬度的化合物为二氧化硅,该化合物的晶体类型为原子晶体,其由Z、Y构成的最小环为12元环,故答案为:原子晶体;12;
(5)体心立方晶胞中铁原子个数=1+8×$\frac{1}{8}$=2;面心立方晶胞中实际含有的Fe原子个数=6×$\frac{1}{6}$+8×$\frac{1}{8}$=4,设体心立方中晶胞的棱长为x,铁原子的直径为A,则3x2=(2A)2,解得x=$\frac{2\sqrt{3}A}{3}$;铁原子直径=A,所以其晶胞体积=R3,面心立方中晶胞的对角线为2A,则其边长=$\sqrt{2}A$,其晶胞体积=2$\sqrt{2}$A3.
体心立方的密度与面心立方的密度之比=$\frac{2m}{(\frac{2\sqrt{3}}{3}{A)}^{3}}$:$\frac{4m}{2\sqrt{2}{A}^{3}}$=3$\root{3}{6}$:8,故答案为:3$\root{3}{6}$:8.
点评 本题综合考查物质结构与性质,涉及核外电子排布规律、杂化理论、等电子体、晶胞的密度等知识点,难点是计算晶胞的密度之比,能正确解答晶胞的体积是解本题的关键,知道体心立方和面心立方中哪三个原子紧密相连即可分析解答,难度中等.

| A. | 950mL,111.2g | B. | 500mL,117g | C. | 1000mL,l17g | D. | 任意规格,117g |
| A. | 稀醋酸与氢氧化钠溶液的反应:H++OH-=H2O | |
| B. | 钠与水反应:Na+H2O=Na++OH-+H2↑ | |
| C. | 氯气与氯化亚铁溶液的反应:Cl2+2Fe2+=2Cl-+2Fe3+ | |
| D. | 碳酸钙溶液与足量稀盐酸的反应:CO32-+2H+=H2O+CO2↑ |
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | PM2.5(2.5微米以下的细颗粒物)主要来自化石燃料的燃烧 | |
| C. | 处理废水时加入明矾作为消毒剂对水进行杀菌消毒 | |
| D. | 某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
(1)
 酚类-OH
酚类-OH(2)
 羧酸-COOH--
羧酸-COOH--(3)
 醛类
醛类
(4)CH3-O-CH3醚类

(5
 酯类
酯类
| A. | (1)(2)(3)(4)(5) | B. | (2)(4) | C. | (2)(3)(4) | D. | (2)(4)(5) |
| A. | 用小苏打作发酵粉焙制糕点 | B. | 用甲醛溶液浸泡海产品 | ||
| C. | 用工业石蜡给水果上蜡“美容” | D. | 用工业酒精勾兑饮用酒 |
 苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.
苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.(1)其制备方法为:

(2)已知:①
| 名称 | 相对分子质量 | 颜色,状态 | 沸点(℃) | 密度(g•cm-3) |
| 苯甲酸 | 122 | 无色片状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 150 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 46 | 无色澄清液体 | 78.3 | 0.7893 |
| 环己烷 | 84 | 无色澄清液体 | 80.8 | 0.7318 |
③无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
(3)实验步骤如下:
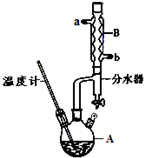
①在仪器A中加入12.20g苯甲酸,25mL 95%的乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按如图所示装好仪器,控制温度在65~70℃加热回流2h.利用分水器不断分离除去反应生成的水,回流环己烷和乙醇.
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热.
③将仪器A内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性.用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,将滤液用蒸馏烧瓶进行分馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分.
④检验合格,测得产品体积为12.86mL.
回答下列问题:
(1)在该实验中,仪器A的名称为三颈烧瓶,其容积最适合的是C(填选项前的字母).
A.25mL B.50mL C.100mL D.250mL
(2)制备苯甲酸乙酯时,最合适的加热方法是水浴加热,控制温度的目的是防止副反应的发生和苯甲酸升华.加入沸石的作用是防暴.
(3)步骤①中使用分水器不断分离除去水的目的是使平衡不断地向正向移动.
(4)步骤②中应控制馏分的温度在C.
A.65~70℃B.78~80℃C.85~90℃D.215~220℃
(5)步骤③有机层应从分液漏斗下口(填“上口”或“下口”)流出.加入Na2CO3的作用是除去硫酸和未反应的苯甲酸;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是苯甲酸乙酯中混有未除净的苯甲酸,在受热至100℃时发生升华.加入氯化钙的目的是使产品中混有的乙醇形成难溶于水的CaCl2•6C2H5OH,过滤除去.
(6)计算本实验的产率为90.02%.

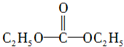 .
.