题目内容
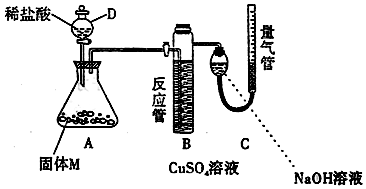
14. 某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.请回答:
某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.请回答:(1)在保证电极反应不变的情况下,能替代Cu做电极的是BD(填字母序号).
A.铝 B.石墨 C.镁 D.铂
(2)M极为阳极,发生反应的电极反应式为Fe-2e-+2OH-=Fe(OH)2;
(3)实验过程中,SO42-从右向左 (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有红褐色斑点产生.
分析 图中,左边装置是原电池,较活泼的金属锌作负极,较不活泼的金属铜作正极,如果要找电极材料代替铜,所找材料必须是不如锌活泼的金属或导电的非金属,M是阳极,N是阴极,电解池中阴极上阳离子得电子发生还原反应,原电池放电时,阴离子向负极移动,据此分析.
解答 解:(1)在保证电极反应不变的情况下,仍然是锌作负极,则正极材料必须是不如锌活泼的金属或导电的非金属,铝是比锌活泼的金属,所以不能代替铜,
故答案为:BD;
(2)N电极连接原电池负极,所以是电解池阴极,M是阳极,发生失电子的氧化反应:Fe-2e-+2OH-=Fe(OH)2;
故答案为:阳;Fe-2e-+2OH-=Fe(OH)2;
(3)原电池放电时,阴离子向负极移动,所以硫酸根从右向左移动,电解池中,阴极上氢离子得电子生成氢气,阳极上铁失电子生成亚铁离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧气氧化生成氢氧化铁,所以滤纸上有红褐色斑点产生,
故答案为:从右向左; 红褐色斑点产生.
点评 本题考查了原电池和电解池原理,侧重于学生的分析能力的考查,注意电解池中如果活泼金属作阳极,则电解池工作时阳极材料失电子发生氧化反应,为易错点,题目难度中等.

练习册系列答案
相关题目
5.为减轻大气污染,可在汽车尾气排放处加装催化转化装置,反应方程式为:2NO(g)+2CO(g)$?_{△}^{催化剂}$2CO2(g)+N2(g).
(1)上述反应使用等质量的某种催化剂时,温度和催化剂的比表面积对化学反应速率的影响对比实验如下表,c(NO)浓度随时间(t)变化曲线如图:
①表中a=1.20×10-3.
②实验说明,该反应是放热反应(填“放热”或“吸热”).
③若在500℃时,投料$\frac{{c({NO})}}{{c({CO})}}=1$,NO的转化率为80%,则此温度时的平衡常数K=第一种情况:设c(NO)=1mol•L-1,则K=160,
第二种情况:设c(NO)=amol•L-1,K=$\frac{160}{a}$,
第三种情况:设n(NO)=amol,容器的容积为V L,则K=$\frac{160V}{a}$.
(2)使用电化学法也可处理NO的污染,装置如图2.已知电解池阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:2HSO3-+2H++2e-=S2O42-+2H2O.吸收池中除去NO的离子方程式为:2NO+2S2O42-+2H2O=N2+4HSO3-.
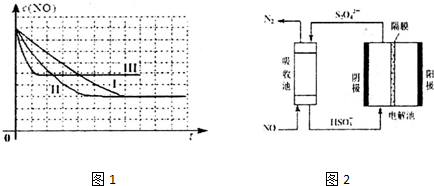
(1)上述反应使用等质量的某种催化剂时,温度和催化剂的比表面积对化学反应速率的影响对比实验如下表,c(NO)浓度随时间(t)变化曲线如图:
| 编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | a | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | b |
②实验说明,该反应是放热反应(填“放热”或“吸热”).
③若在500℃时,投料$\frac{{c({NO})}}{{c({CO})}}=1$,NO的转化率为80%,则此温度时的平衡常数K=第一种情况:设c(NO)=1mol•L-1,则K=160,
第二种情况:设c(NO)=amol•L-1,K=$\frac{160}{a}$,
第三种情况:设n(NO)=amol,容器的容积为V L,则K=$\frac{160V}{a}$.
(2)使用电化学法也可处理NO的污染,装置如图2.已知电解池阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:2HSO3-+2H++2e-=S2O42-+2H2O.吸收池中除去NO的离子方程式为:2NO+2S2O42-+2H2O=N2+4HSO3-.

19.下列观点,正确的是( )
| A. | 化学研究会造成严重的环境污染,危害人们的生活 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| C. | 用大量木材作燃料可以缓解当前能源不足问题 | |
| D. | 对于常见的大多数金属,其金属活动性越强,冶炼就越困难 |
6.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 9.2g甲酸中,所含化学键的数目为0.8 NA | |
| B. | 常温下,28g Fe与足量的浓硝酸反应,转移的电子数为1.5NA | |
| C. | 标准状况下,2.24LNH3和CH4的混合气体,所含电子总数为NA | |
| D. | 标准状况下,22.4L己烷所含有的分子数目为NA |