题目内容
17.比较1mol N2和1mol CO的下列物理量:①质量 ②分子总数 ③原子总数 ④体积,其中一定相同的是( )| A. | ① | B. | ①② | C. | ①②③ | D. | ②③④ |
分析 氮气和一氧化碳气体的摩尔质量相等,二者都是双原子分子,根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$可知等物质的量的N2和CO的质量、分子总数、原子总数相等;由于没有告诉在相同条件下,则无法比较二者体积大小.
解答 解:M(N2)=28g/mol,M(CO)=28g/mol,二者摩尔质量相同,则由m=nM可知质量相同,①正确;
二者都是双原子分子,则等物质的量时,分子总数、原子总数相同,则②③正确;
由于气体存在的条件未知,则等物质的量时体积不一定相等,④错误.
故选C.
点评 本题考查阿伏伽德罗定律及其推论,为高考高频考点,侧重于学生的分析能力和计算能力的考查,相关计算公式的运用以及气体存在的条件,为易错点,难度不大.

练习册系列答案
相关题目
14.短周期主族元素X、Y、Z、W的原子序数依次递减,四种元素中没有同族元素,其原子的最外层电子数之和为15,W与X、Y、Z位于相邻周期,X原子的最外层电子数是W原子内层电子总数的3倍,单质Z可与水剧烈反应,Y、Z均为金属元素.下列叙述正确的是( )
| A. | 原子半径:Y>Z | |
| B. | 单质熔点:W>X | |
| C. | X、Y的氧化物均能与Z的氧化物对应的水化物反应 | |
| D. | X、W的最简单氢化物的水溶液均显酸性 |
8.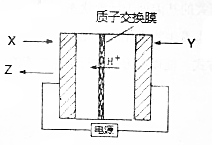 氨是生产氮肥、尿素等物质的重要原料,电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )
氨是生产氮肥、尿素等物质的重要原料,电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )
 氨是生产氮肥、尿素等物质的重要原料,电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )
氨是生产氮肥、尿素等物质的重要原料,电化学法是合成氨的一种新方法,其原理如图所示,下列有关说法正确的是( )| A. | 图中所示物质中,X为H2,Y为N2 | |
| B. | Y参与的电极反应为H2+2e-═2H+ | |
| C. | 当有3gH+通过质子交换膜时,Z的体积为22.4L | |
| D. | 反应过程中左边区域溶液PH逐渐升高 |
12.25℃时,1mol/L醋酸加水稀释至0.01mol/L,下列变化正确的是( )
| A. | 溶液中c(OH-)减小 | B. | pH的变化值小于2 | ||
| C. | 溶液中H+的数目减小 | D. | Kw的值增大 |
9.下列离子方程式书写正确的是( )
| A. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 氯气与水反应:Cl2+H2O═H++Cl-+HClO |
6.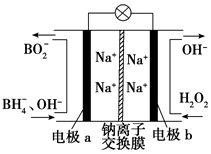 据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示.下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示.下列说法正确的是( )
 据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示.下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3)和H2O2作原料的燃料电池可用作空军通信卫星电源,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示.下列说法正确的是( )| A. | 每消耗1 mol H2O2,转移的电子为1 mol | |
| B. | 电极b采用MnO2,MnO2既作电极材料又有催化作用 | |
| C. | 该电池的正极反应为BH4-+8OH--8e-═BO2-+6H2O | |
| D. | 电池放电时Na+从b极区移向a极区 |
7.下列物质中,既能发生氧化反应,又能发生还原反应,还能发生水解反应的是( )
| A. | CH2═CH2 | B. | CH3CH2CHO | C. | CH3COOH═CH2 | D. | CH3CH(OH)CH3 |