题目内容
12.25℃时,1mol/L醋酸加水稀释至0.01mol/L,下列变化正确的是( )| A. | 溶液中c(OH-)减小 | B. | pH的变化值小于2 | ||
| C. | 溶液中H+的数目减小 | D. | Kw的值增大 |
分析 醋酸溶液中存在CH3COOH?CH3COO-+H+,加水稀释促进电离,n(CH3COO-)和n(H+)增大,n(CH3COOH)减小,结合溶液体积变化以及物质的量之比等于浓度之比解答该题.
解答 解:A.对醋酸加水稀释,溶液中的氢离子浓度减小,而Kw不变,故c(OH-)增大,故A错误;
B.加水稀释,醋酸的电离被促进,电离出的氢离子的物质的量增多,故pH的变化小于2,故B正确;
C.稀释后醋酸的电离程度增大,则溶液中氢离子的数目增多,故C错误;
D.Kw只受温度的影响,温度不变,Kw的值不变,故加水稀释对Kw的值无影响,故D错误.
故选B.
点评 本题考查了弱电解质的电离及其影响,题目难度中等,明确影响电离平衡的因素为解答关键,注意水的离子积只受温度影响,为易错点,试题培养了稀释的分析能力及灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.化学与科技、生产、生活等密切相关,下列说法正确的是( )
| A. | 中国的圆珠笔头一直需要进口笔尖钢,经过5年数不清的失败,2016年9月,中国太钢集团利用家常和面原理在钢水中加入添加剂试验成功,造出圆珠笔头,可完全替代进口.由此信息可知笔尖钢为合金,且具有良好的切削性 | |
| B. | 日前从中国建筑材料科学研究总院获悉,天宫二号采用了该院研发改进的新材料,耐辐射石英玻璃,其主要成分为硅 | |
| C. | 用废轮胎、废电缆打碎制成的塑胶跑道,可以提高原子利用率 | |
| D. | 塑化剂DEHP邻苯二甲酸二(2-乙基)己脂,对人体无害,可用作食品添加剂 |
3.对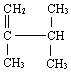 的命名正确的是( )
的命名正确的是( )
 的命名正确的是( )
的命名正确的是( )| A. | 3-乙烯基-2-甲基丁烷 | B. | 2,3-二甲基-3-丁烯 | ||
| C. | 2,3-二甲基丁烯 | D. | 2,3-二甲基-1-丁烯 |
7.下列电离方程式错误的是( )
| A. | (NH4)2SO4溶于水:(NH4)2SO4═2NH4++SO42- | |
| B. | Fe(OH)3溶于水:Fe(OH)3═3OH-+Fe3+ | |
| C. | HF溶于水:HF?H++F- | |
| D. | NaHS溶于水:NaHS=Na++HS-,HS-?H++S2- |
17.比较1mol N2和1mol CO的下列物理量:①质量 ②分子总数 ③原子总数 ④体积,其中一定相同的是( )
| A. | ① | B. | ①② | C. | ①②③ | D. | ②③④ |
4.下列关于镭(第七周期的IIA族)的性质的描述中不正确的是( )
| A. | 在化合物中呈+2价 | B. | 氢氧化物呈两性 | ||
| C. | 单质使水分解,放出氢气 | D. | 碳酸盐难溶于水 |
1.下列各物质中的少量杂质,可用括号内的试剂和方法除去的是( )
| A. | 苯中溶有苯酚(浓溴水,过滤) | B. | 溴苯中溶有溴(苯,分液) | ||
| C. | CO2中含有SO2(KMnO4酸性溶液,洗气) | D. | 乙醇中含有水(金属钠,蒸馏) |
2.下列关于有机化合物的说法正确的是 ( )
| A. | 分子式为C3H6Cl2的有机物有4种同分异构体 | |
| B. | 包装用材料聚乙烯分子中含有碳碳双键 | |
| C. | 乙炔和溴的四氯化碳溶液反应成1,2-二溴乙烷 | |
| D. | 油脂与NaOH浓溶液反应制高级脂肪酸钠属于加成反应 |
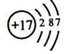 .
.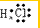 ;由两种元素组成的共价化合物的水溶液呈碱性,这种化合物的结构式为
;由两种元素组成的共价化合物的水溶液呈碱性,这种化合物的结构式为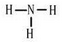 ,四种元素对应的化学性质最稳定的单质的电子式为
,四种元素对应的化学性质最稳定的单质的电子式为 .
.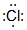 →
→ .
.