题目内容
18.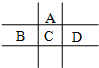 有A、B、C、D、E五种短周期元素,已知A、B、C、D四种元素在周期表中的位置如图所示,其中C元素的最高价氧化物对应的水化物浓溶液是一种常见的干燥剂.D在海水中大量富集.E的氧化物是两性氧化物,回答下列问题:
有A、B、C、D、E五种短周期元素,已知A、B、C、D四种元素在周期表中的位置如图所示,其中C元素的最高价氧化物对应的水化物浓溶液是一种常见的干燥剂.D在海水中大量富集.E的氧化物是两性氧化物,回答下列问题:(1)写出元素的符号:BP,CS,DCl.
(2)C单质在A单质中燃烧的产物通入品红溶液,反应现象品红溶液褪色.
(3)A与E形成的化合物的化学式是Al2O3.
分析 A、B、C、D、E五种短周期元素,已知A、B、C、D四种元素在周期表中的位置如图所示,其中C元素的最高价氧化物对应的水化物浓溶液是一种常见的干燥剂,该干燥剂为浓硫酸,则C为S元素;结合各元素的相对位置可知,A为O、B为P、D为Cl元素;D为Cl,Cl在海水中大量富集,满足条件;E的氧化物是两性氧化物,则E为Al元素,据此进行解答.
解答 解:已知A、B、C、D四种元素在周期表中的位置如图所示,其中C元素的最高价氧化物对应的水化物浓溶液是一种常见的干燥剂,该干燥剂为浓硫酸,则C为S元素;结合各元素的相对位置可知,A为O、B为P、D为Cl元素;D为Cl,Cl在海水中大量富集,满足条件;E的氧化物是两性氧化物,E为短周期元素,该氧化物为氧化铝,则E为Al元素,
(1)根据分析可知,B为P、C为S、D为Cl元素,
故答案为:P;S;Cl;
(2)C单质在A单质中燃烧的产物为SO2,SO2具有漂白性,将SO2气体通入品红溶液中,会观察到品红溶液褪色,
故答案为:品红溶液褪色;
(3)A为O、E为Al,二者形成的化合物为氧化铝,化学式为:Al2O3,
故答案为:Al2O3.
点评 本题考查了位置、结构与性质关系的应用,题目难度不大,推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
3.实验报告中,以下数据和所用仪器合理的是( )
| A. | 用托盘天平称取11.7gNaCl | |
| B. | 用50mL量筒量取21.48mL稀硫酸 | |
| C. | 用碱式滴定管量取25.03mLH2SO4溶液 | |
| D. | 用pH试纸测定HNO3溶液的pH=3.7 |
4.电解100ml含c(H+)=0.40mol/L的下列溶液.当电路中通过0.04mol电子时,理论上析出金属质量最大的是( )
| A. | 0.10mol/L Ag+ | B. | 0.20mol/L Zn2+ | C. | 0.20mol/L Cu2+ | D. | 0.20mol/L Pb2+ |
13.原子序数为12和16的两种元素,它们的最高价氧化物对应的水化物分别是( )
| A. | Ca(OH)2、H2SO4 | B. | Mg(OH)2、H2SO4 | C. | KOH、HCl | D. | Al(OH)3、H3PO4 |
10.下列关于糖类、蛋白质、油脂和维生素的说法中,正确的是( )
| A. | 它们的组成都含有C、H、O、N等元素 | |
| B. | 在一定条件下,都能发生水解反应 | |
| C. | 蛋白质和氨基酸一样具有两性 | |
| D. | 淀粉溶液中加稀硫酸加热水解后,加入新制银氨溶液加热可以产生银镜 |
 .
.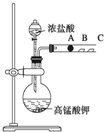 某研究性学习小组设计了一组实验来探究元素周期律.甲同学设计了如图装置来验证卤族元素性质的递变规律.A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.
某研究性学习小组设计了一组实验来探究元素周期律.甲同学设计了如图装置来验证卤族元素性质的递变规律.A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.