题目内容
16.如图是电解熔融 NaCl 制备金属钠的装置示意图,下列有关判断正确的是( )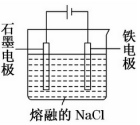
| A. | 通过该装置可以将化学能转化为电能 | |
| B. | 石墨电极为正极 | |
| C. | Na+在铁电极上得到电子被还原为钠 | |
| D. | 电流从负极流出,流入铁电极 |
分析 A.该装置为电解池,是将电能转化成化学能的装置;
B.石墨电解与电源正极相连,为电解池的阳极;
C.铁电极为阴极,钠离子在铁电极得到电子生成金属钠;
D.电流从电源的正极流出,流入铁电极.
解答 解:A.该装置是电解熔融NaCl 制备金属钠的装置,是将电能转化成化学能,故A错误;
B.石墨电极连接的是正极,则说明为该电解池的阳极,故B错误;
C.Fe电极为电解池的阴极,Na+在铁电极上得到电子被还原为钠,故C正确;
D.电流从原电池的正极流出,负极流入,所以该装置中电流从正极流向石墨,故D错误;
故选C.
点评 本题考查了电解原理及其应用,题目难度不大,正确判断电解池的两极为解答关键,注意熟练掌握原电池工作原理,试题培养了学生的分析能力及灵活应用.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
8. 近期微信热传的“苯宝宝表情包”是一系列苯的衍生物配以相应文字形成的(如图所示).其中
近期微信热传的“苯宝宝表情包”是一系列苯的衍生物配以相应文字形成的(如图所示).其中 属于( )
属于( )
 近期微信热传的“苯宝宝表情包”是一系列苯的衍生物配以相应文字形成的(如图所示).其中
近期微信热传的“苯宝宝表情包”是一系列苯的衍生物配以相应文字形成的(如图所示).其中 属于( )
属于( )| A. | 氧化物 | B. | 醇类 | C. | 羧酸 | D. | 酚类 |
4.下列关于Na2CO3和NaHCO3性质的叙述中,不正确的是( )
| A. | 加入澄清石灰水都有白色沉淀生成 | |
| B. | 向NaOH溶液中通入过量的CO2可制得NaHCO3 | |
| C. | 向饱和Na2CO3溶液中通入足量的CO2没有明显现象 | |
| D. | 可利用稀盐酸来区别Na2CO3、NaHCO3两种无色溶液 |
11.下列关于物质的量浓度表述正确的是( )
| A. | 0.3mol•L-1 的Na2SO4溶液中含有Na+和SO42-的总物质的量为0.9mol | |
| B. | 当1L水吸收22.4L氨气时所得氨水的浓度不是1mol•L-1,只有当22.4L氨气溶于水制得1L氨水时,其浓度是1mol•L-1 | |
| C. | 在K2SO4和NaCl的混合溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同 | |
| D. | 250g胆矾溶于水得到1L溶液,所得CuSO4溶液的物质的量浓度为1mol•L-1 |
1.现有a、b、c三个容器,a容器恒容恒温,b容器恒压恒温,c容器恒容绝热.在三个容器中各充入1mol I2(g)和2mol H2发生反应I2(g)+H2(g)?2HI(g)△H<0,初始时三个容器的体积和温度均相等,则反应达到平衡后,三个容器中I2(g)的转化率的大小关系是( )
| A. | a=b>c | B. | b>a>c | C. | c>b>a | D. | a=b<c |
8.某无色溶液能与铝作用生成氢气,则溶液中可能大量共存的离子组是:( )
| A. | H+、Ba2+、Mg2+、Cl- | B. | Cl-、CO32-、Cu2+、Mg2+ | ||
| C. | NO3-、SO42-、K+、H+ | D. | NO3-、OH-、Ba2+、Cl- |
6.均为0.5mol•L-1的下列物质的溶液,从常温加热到80℃,其pH没有明显变化的是( )
| A. | NaHSO4 | B. | NaOH | C. | CH3COONa | D. | NH4Cl |