题目内容
4.下列关于Na2CO3和NaHCO3性质的叙述中,不正确的是( )| A. | 加入澄清石灰水都有白色沉淀生成 | |
| B. | 向NaOH溶液中通入过量的CO2可制得NaHCO3 | |
| C. | 向饱和Na2CO3溶液中通入足量的CO2没有明显现象 | |
| D. | 可利用稀盐酸来区别Na2CO3、NaHCO3两种无色溶液 |
分析 A.Na2CO3和NaHCO3都能与澄清的石灰水反应生成沉淀;
B.氢氧化钠与过量二氧化碳反应生成碳酸氢钠;
C.向饱和Na2CO3溶液中通入足量的CO2可生成碳酸氢钠沉淀;
D.Na2CO3、NaHCO3与盐酸反应的剧烈程度不同.
解答 解:A.Na2CO3和NaHCO3都能与澄清的石灰水反应生成碳酸钙沉淀,故A正确;
B.氢氧化钠与过量二氧化碳反应生成碳酸氢钠,二氧化碳不足时生成碳酸钠,故B正确;
C.在饱和Na2CO3溶液中通入过量二氧化碳气体可得到NaHCO3沉淀,故C错误;
D.分别滴加HCl溶液,反应离子方程式为CO32-+2H+═CO2↑+H2O,HCO3-+H+═H2O+CO2↑,相同条件下NaHCO3比Na2CO3反应放出气体剧烈,故D正确.
故选C.
点评 本题考查Na2CO3和NaHCO3性质的异同,为高频考点,题目难度不大,注意把握Na2CO3和NaHCO3性质,选项D为解答的易错点,注重基础知识的积累.

练习册系列答案
 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
16.用CCl4提取碘水中碘的装置如图所示,下列说法不正确的是( )


| A. | 实验过程包括:萃取、分液 | |
| B. | 右图下层为CCl4层,呈紫色 | |
| C. | 用酒精也能够提取碘水中的碘 | |
| D. | 用汽油洗涤洒在衣物上的油汤也是一种萃取 |
12.下列有关叙述正确的是( )
| A. | 电泳现象可证明胶体带电荷 | |
| B. | 直径在1~100mm之间的粒子称为胶体 | |
| C. | 是否具有丁达尔效应是溶液和胶体的本质区别 | |
| D. | 胶体粒子很小,可以透过滤纸 |
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 22g N2O和CO2的混合物中所含电子数为11NA | |
| B. | 12g石墨烯(单层石墨)中含有C-C键的数目为3NA | |
| C. | 与铁反应时,消耗22.4L(标准状况)Cl2转移的电子数定为3NA | |
| D. | 若1L 0.2mol•L-1的FeCl3溶液完全水解形成胶体,则胶休微粒数为0.2NA |
9.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| C. | Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O=2AlO2-+3H2↑ | |
| D. | Al2(SO4)3溶液滴加过量NaOH溶液:Al3++3OH-=Al(OH)3↓ |
16.如图是电解熔融 NaCl 制备金属钠的装置示意图,下列有关判断正确的是( )
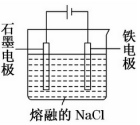

| A. | 通过该装置可以将化学能转化为电能 | |
| B. | 石墨电极为正极 | |
| C. | Na+在铁电极上得到电子被还原为钠 | |
| D. | 电流从负极流出,流入铁电极 |
13.已知X、Y、Z、W(含同一元素)有如图所示的转化关系,若X是一种单质,W为一种含氧酸,则X不可能是( )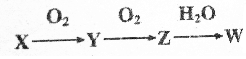
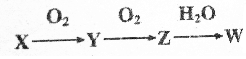
| A. | Na | B. | S | C. | C | D. | Si |