题目内容
18.NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 26g的苯和乙炔的混合物最多可以与2mol的氢气发生加成 | |
| B. | 某温度下,MgCO3的Ksp=4×10-6,则饱和溶液中含Mg2+数目为2×10-3NA | |
| C. | 标准状况下,NA个NO分子和0.5NA个O2分子充分反应后气体体积为22.4 L | |
| D. | 氢气与氯气反应生成标准状况下22.4 L氯化氢,断裂化学键总数为1NA |
分析 A、苯的摩尔质量为乙炔的三倍,和氢气加成时消耗氢气的量也是乙炔的三倍;
B、溶液体积不明确;
C、标准状况下,NA个NO分子和0.5NA个O2分子充分反应后生成1molNO2,但NO2中存在平衡:2NO2?N2O4;
D、根据反应H2+Cl2=2HCl可知,当生成2molHCl时,断裂2mol化学键.
解答 解:A、苯的摩尔质量为乙炔的三倍,和氢气加成时消耗氢气的量也是乙炔的三倍,故混合物可以认为是由“C2H2”构成的,故26g混合物中含有的“C2H2”的物质的量为1mol,则能和1mol氢气加成,故A错误;
B、溶液体积不明确,故饱和溶液中的镁离子的个数无法计算,故B错误;
C、标准状况下,NA个NO分子和0.5NA个O2分子充分反应后生成1molNO2,但NO2中存在平衡:2NO2?N2O4,导致分子个数和体积变小,故后来气体体积小于22.4L,故C错误;
D、根据反应H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl可知,当生成2molHCl时,断裂2mol化学键,故当生成标况下22.4LHCl即1molHCl时,断裂NA个共价键,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.如表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题.
(1)元素④的名称是氧,从元素原子得失电子的角度看,元素④具有氧化性(填“氧化性”、“还原性”);
(2)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:H2O>H2S>PH3(写氢化物的化学式);
(3)元素③④⑤形成的离子半径由大到小的顺序是N3->O2->Na+(用离子符号表示)
(4)元素⑦的原子结构示意图是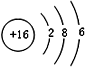 ;
;
(5)最高价氧化物对应水化物酸性最强的酸是HClO4,化学性质最稳定的是Ne金属性最强的元素是Na(用化学符号表示)
| ⅠA | ⅧA | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑧ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ | ||||
(1)元素④的名称是氧,从元素原子得失电子的角度看,元素④具有氧化性(填“氧化性”、“还原性”);
(2)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:H2O>H2S>PH3(写氢化物的化学式);
(3)元素③④⑤形成的离子半径由大到小的顺序是N3->O2->Na+(用离子符号表示)
(4)元素⑦的原子结构示意图是
 ;
;(5)最高价氧化物对应水化物酸性最强的酸是HClO4,化学性质最稳定的是Ne金属性最强的元素是Na(用化学符号表示)
9.下列物质中只含有离子键的是( )
| A. | MgCl2 | B. | NH4Cl | C. | CO2 | D. | NaOH |
3.下列说法正确的是( )
| A. | 在SiO2晶体中,1个Si原子和2个O原子形成两条共价键 | |
| B. | 由多种非金属元素组成的化合物一定是共价化合物 | |
| C. | HF、HCl、HBr、HI四种物质的沸点依次升高 | |
| D. | 晶体熔化时化学键不一定发生断裂 |
10.25℃时,某溶液中由水电离出的c(OH-)=1×10-13mol/L,该溶液中一定不能大量共存的离子组是( )
| A. | NH4+、Fe3+、SO42-、Cl- | B. | CO32-、PO43-、K+、Na+ | ||
| C. | Na+、SO42-、NO3-、Cl- | D. | HCO3-、Na+、HSO3-、K+ |
7.下列物质属于弱电解质的是( )
| A. | H2SO4 | B. | NaCl | C. | NaOH | D. | CH3COOH |
8.向一密闭容器中充入1mol N2和3mol H2,在一定条件下反应发生,下列有关说法正确的是( )
| A. | 达到化学平衡时,N2将完全转化为NH3 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度之比为l:3:2 | |
| C. | 达到化学平衡时'容器内气体的平均摩尔质量不再变化 | |
| D. | 达到化学平衡时,正反应和逆反应的速率都为零 |