题目内容
17.在标准状况下,跟11.2L氨气中所含的氢原子数相同的下列物质是( )| A. | 标准状况8.4LCH4 | B. | 0.3molHCl | C. | 98gH3PO4 | D. | 18gH2O |
分析 根据n=$\frac{V}{{V}_{m}}$计算出标况下11.2L氨气的物质的量,根据N=nNA可知所含的氢原子数相同时含有H的物质的量相同,分别计算出各物质含有H的物质的量,根据计算结果进行判断.
解答 解:标况下11.2L氨气的物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,0.5mol氨气分子中含有H的物质的量为:0.5mol×3=1.5mol,根据N=nNA可知所含的氢原子数相同时含有H的物质的量应该为1.5mol,
A.标准状况8.4LCH4中含有H的物质的量为:$\frac{8.4L}{22.4L/mol}$×4=1.5mol,故A正确;
B.0.3molHCl中含有0.3molH原子,故B错误;
C.98gH3PO4中含有H的物质的量为:$\frac{98g}{98g/mol}$×3=3mol,故C错误;
D.18gH2O中含有H的物质的量为:$\frac{18g}{18g/mol}$×2=2mol,故D错误;
故选A.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与其它物理量之间的关系即可解答,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
相关题目
7.下表是元素周期表的一部分,针对表中的①~⑨中元素,按要求用相应的化学用语填空回答.
(1)①为铍(填元素名称),在这些元素中,非金属性最强的元素Ar(填元素符号),化学性质最不活泼的原子的原子结构示意图为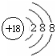 .
.
(2)③⑤⑦元素形成的简单离子,离子半径由小到大的顺序Al3+<F-<Cl-(离子符号表示)
(3)④⑦元素形成的化合物的电子式为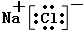
(4)用化学式,“<”或“>”比较,②③两元素气态氢化物的稳定性NH3<HF;⑦⑨两元素最高价氧化物对应水化物酸性H3PO4<HClO4.
(5)④⑤两元素最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑨ | ⑦ | ⑧ |
 .
.(2)③⑤⑦元素形成的简单离子,离子半径由小到大的顺序Al3+<F-<Cl-(离子符号表示)
(3)④⑦元素形成的化合物的电子式为
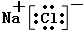
(4)用化学式,“<”或“>”比较,②③两元素气态氢化物的稳定性NH3<HF;⑦⑨两元素最高价氧化物对应水化物酸性H3PO4<HClO4.
(5)④⑤两元素最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
5.下列有关乙醇的说法正确的是( )
| A. | 属于高分子化合物 | B. | 能被强氧化剂氧化 | ||
| C. | 能使石蕊试液变红 | D. | 与CH3OCH3化学性质相同 |
12.同温同压下,某容器充满氧气时重116g,若充满CO2时重122g.现充满X气体时重114g,则X气体不可能是( )
| A. | CO | B. | N2 | C. | C2H4 | D. | HCl |
2.化学与人们的日常生活密切相关,下列叙述正确的是( )
| A. | 鸡蛋清溶液中加入CuSO4溶液,有沉淀析出,该性质可用于蛋白质的分离与提纯 | |
| B. | 明矾净水时发生了化学及物理变化,能起到杀菌、消毒的作用 | |
| C. | 淀粉溶液、豆浆、碳素墨水均可发生丁达尔现象 | |
| D. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 |
9.已知H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别是-285.8kJ•mol-1、-1411.0kJ•mol-1和-1366.8kJ•mol-1,( C2H4、C2H5OH(l)充分燃烧后的产物为CO2和H2O(l)),则由C2H4(g)和H2O(I)反应生成C2H5OH(1)的△H为( )
| A. | -44.2kJ•mol-1 | B. | +44.2kJ•mol-1 | C. | -330kJ•mol-1 | D. | +330kJ•mol-1 |
6.已知丁基(-C4H9)有四种结构,某烃的结构简式为 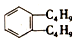 ,该烃可能的结构有( )
,该烃可能的结构有( )
 ,该烃可能的结构有( )
,该烃可能的结构有( )| A. | 16种 | B. | 14种 | C. | 12种 | D. | 10种 |
7. 某兴趣小组设计简易原电池装置如图所示,该电池工作时,下列说法正确的是( )
某兴趣小组设计简易原电池装置如图所示,该电池工作时,下列说法正确的是( )
 某兴趣小组设计简易原电池装置如图所示,该电池工作时,下列说法正确的是( )
某兴趣小组设计简易原电池装置如图所示,该电池工作时,下列说法正确的是( )| A. | 锌片做正极 | B. | 碳棒上有气泡产生 | ||
| C. | 可将电能转化为化学能 | D. | 电子由碳棒经导线流向锌片 |