题目内容
2.硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质.用硼泥生产氢氧化镁的工艺流程如图所示,已知生成氢氧化物沉淀的pH见表.下列说法正确的是( )
| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| A. | 反应①中H2O2主要用于还原剂 | |
| B. | 滤渣1和滤渣2都不能溶于NaOH溶液 | |
| C. | 反应③发生主要反应的离子方程式:H++OH-═H2O | |
| D. | 以滤渣2为原料可以制备涂料铁红 |
分析 硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质,由流程可知,加入硫酸,Fe2O3、FeO、Al2O3都和硫酸反应,SiO2不与硫酸反应,滤渣1为SiO2,过氧化氢具有氧化性,加入的过氧化氢可把亚铁离子氧化成铁离子,加入氢氧化钠,溶液pH为6,铁离子生成氢氧化铁沉淀,铝离子和氢氧根离子形成氢氧化铝沉淀,过滤得到的滤渣2为Fe(OH)3、Al(OH)3,滤液2中含镁离子,调节pH=12,得到滤渣3为Mg(OH)2,洗涤烘干得到Mg(OH)2晶体,以此来解答.
解答 解:A.由上述分析可知,①中发生H2O2+2Fe2++2H+═2Fe3++2H2O,H2O2作氧化剂,故A错误;
B.滤渣1中二氧化硅、滤渣2中Al(OH)3都能溶于NaOH溶液,故B错误;
C.反应③调节pH=12,使镁离子转化为沉淀,发生Mg2++2OH-═Mg(OH)2↓,故C错误;
D.滤渣2含Fe(OH)3,加热得到氧化铁,则可以制备涂料铁红,故D正确;
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握流程中发生的反应、混合物分离提纯方法、元素化合物知识为解答的关键,侧重分析与实验能力的考查,注意氢氧化物沉淀的pH应用,题目难度不大.

练习册系列答案
相关题目
13.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
| B | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| C | 向含有酚酞的Na2CO3溶液中加入少量的BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| D | 向亚硫酸钠试样中滴入盐酸酸化的Ba(ClO)2溶液 | 产生白色沉淀 | 试样已氧化变质 |
| A. | A | B. | B | C. | C | D. | D |
10.在一容积为2L的恒温恒容密闭容器中充入2mol SO2和1mol O2,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ•mol-l (Q>O),下列有关说法不正确的是( )
| A. | 反应达到平衡时,放出热量为QkJ | |
| B. | 若容器的压强不再发生交化,则反应达到平衡 | |
| C. | 反应过程中c(SO2)+c(SO3)=1 mol•L-1恒成立 | |
| D. | 平衡时,SO2、O2的转化率相等 |
17.汽车安全气囊弹出时的反应为:10NaN3+2KNO3+6SiO2$\frac{\underline{\;撞击\;}}{\;}$5Na2SiO3+K2SiO3+16N2↑.下列说法正确的是( )
| A. | 自然界中氮、钠、硅元素均可以游离态形式存在 | |
| B. | 将反应后的固体溶于适量水,静置,通入CO2,无现象 | |
| C. | 微粒的半径:r(K+)>r(Na+)>r(O2-) | |
| D. | 若反应中转移6.02×1022电子,则消耗NaN3的质量为6.5g |
7.化学与生产、生活、社会发展等息息相关,下列说法正确的是( )
| A. | 煤经过气化、液化等物理变化可转变为清洁燃料 | |
| B. | 在食品包装时放入盛有铁粉的透气小袋可防止食品氧化变质 | |
| C. | 为补充土壤中的钾元素,可在田间焚烧桔秆 | |
| D. | 聚乙烯、聚氯乙烯均可作包装材料,且不会造成环境污染 |
14.化学与生活、社会发展息息相关.下列说法正确的是( )
| A. | 自来水中加入氯气与污水中加入明矾的原理相同 | |
| B. | 汽油、甘油、花生油均能发生水解反应和氧化反应 | |
| C. | 硫酸铜溶液可用于游泳池的消毒是利用了Cu2+能使蛋白质盐析 | |
| D. | 现代工业生产中的芳香烃来源于石油的催化重整和煤的干馏 |
11.酚醛树脂M结构如图,下列说法不正确的是( )


| A. | M是合成高分子化合物 | B. | n是一个定值 | ||
| C. | 可用苯酚和甲醛合成M | D. | 合成M的反应缩聚反应 |
13.A、B、C、D、E五种元素,前四种短周期元素在周期表中的相对位置如图所示,酸雨的形成与D元素密切相关,E2+的核外电子数比D原子的核外电子数多2,下列说法正确的是( )
| A | B | C |
| D |
| A. | 原子半径由大到小的顺序为E>B>D>C>A | |
| B. | 元素D可形成多种酸,它们的酸根均能促进水的电离 | |
| C. | EB2中存在离子键与非极性共价键 | |
| D. | C位于周期表中第二周期第ⅦA族,其最高正价为+7 |
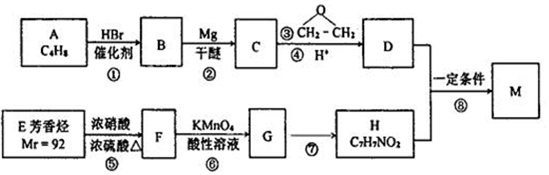
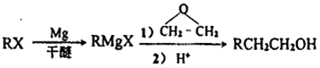
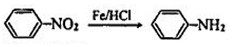 (苯环上的-NH2易被氧化).
(苯环上的-NH2易被氧化).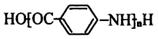 .
.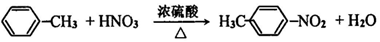 .
. .
. .
.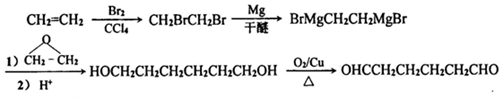 .
.