题目内容
17.汽车安全气囊弹出时的反应为:10NaN3+2KNO3+6SiO2$\frac{\underline{\;撞击\;}}{\;}$5Na2SiO3+K2SiO3+16N2↑.下列说法正确的是( )| A. | 自然界中氮、钠、硅元素均可以游离态形式存在 | |
| B. | 将反应后的固体溶于适量水,静置,通入CO2,无现象 | |
| C. | 微粒的半径:r(K+)>r(Na+)>r(O2-) | |
| D. | 若反应中转移6.02×1022电子,则消耗NaN3的质量为6.5g |
分析 A.根据钠很活泼,硅为亲氧元素分析;
B.根据碳酸酸性比硅酸强判断;
C.根据核外电子层数越大半径最大,核外电子层相同,核电荷数越大,半径越小判断;
D.每消耗NaN310mol,该反应中转移2×(5-0)=10e-,据此计算.
解答 解:A.因为钠很活泼,硅为亲氧元素,所以自然界中钠、硅元素均以化合态形式存在,故A错误;
B.因为碳酸酸性比硅酸强,所以将反应后的固体溶于适量水,静置,通入CO2,会有硅酸沉淀生成,故B错误;
C.因为K+核外电子为三层半径最大,而Na+、O2-核外电子均为两层,又钠离子核电荷数大于氧离子,所以半径氧离子大于钠离子,所以微粒的半径:r(K+)>r(O2-)>r(Na+),故C错误;
D.每消耗NaN310mol,该反应中转移2×(5-0)=10e-,所以若反应中转移6.02×1022电子,则消耗NaN3的质量为6.5g,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意从化合价角度分析,将N3-作为整体来分析为解答的难点,题目难度中等.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
15.1L0.1mol/LNH4Cl溶液中加入或通入物质后溶液导电性无明显变化的是( )
| A. | 0.1molHCl气体 | B. | 0.1molNa2SO4固体 | ||
| C. | 0.2molNaOH固体 | D. | 0.1mol葡萄糖晶体 |
8.常温下,下列有关电解质溶液的说法正确的是( )
| A. | 含有AgBr和AgI固体的悬浊液:c(Ag+)>c(Br-)=c(I-) | |
| B. | 25℃时,0.1mol•L-1醋酸溶液PH=a,0.01mol•L-1醋酸溶液PH=b,则b=a+1 | |
| C. | 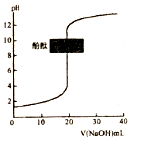 常温下,图表示以酚酞作指示剂,用0.1mol•L-1NaOH溶液滴定未知浓度的盐酸,滴定至终点时,溶液一定呈中性 | |
| D. | 向0.1mol•L-1的氨水中加入硫酸铵固体,则溶液中c(OH-)/c(NH3•H2O)减小 |
5.化合物X是一种黄酮类化合物的中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( )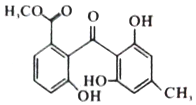

| A. | 化合物X分子式为C16H12O6 | |
| B. | 化合物X含有醚健、羰基,羟基三种官能团 | |
| C. | lmol化合物X最多可与4mol Br2发生反应 | |
| D. | lmol化合物X最多能与3mol NaOH反应 |
2.硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质.用硼泥生产氢氧化镁的工艺流程如图所示,已知生成氢氧化物沉淀的pH见表.下列说法正确的是( )


| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| A. | 反应①中H2O2主要用于还原剂 | |
| B. | 滤渣1和滤渣2都不能溶于NaOH溶液 | |
| C. | 反应③发生主要反应的离子方程式:H++OH-═H2O | |
| D. | 以滤渣2为原料可以制备涂料铁红 |
9.化学与生产、生活、社会等密切相关,下列说法正确的是( )
| A. | 人民币防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料 | |
| B. | “地沟油”禁止食用,但可以用来制肥皂,也可以通过分馏提取得到汽油 | |
| C. | 氟利昂作制冷剂会加剧雾霾天气的形成 | |
| D. | NH4HCO3受热能分解产生气体,在食品工业中可作为焙制糕点的膨松剂 |
6.对下列现象或事实的化学解释不正确的是( )
| 选项 | 现象或事实 | 化学解释 |
| A | 节日焰火五彩缤纷 | 金属化合物的焰色反应 |
| B | 工业上通过煤的干馏制备焦炭 | 煤的干馏是物理过程 |
| C | 用热的纯碱溶液洗去油污 | Na2CO3溶于水显碱性 |
| D | 用浸泡过高锰酸钾溶液的硅土保鲜水果 | 乙烯被酸性高锰酸钾氧化 |
| A. | A | B. | B | C. | C | D. | D |
8.短周期主族元素W、X、Y、Z的原子序数依次增大,W2-和X+的电子层结构相同,X的原子半径是短周期主族元素原子中最大的,W与Y同族.下列说法正确的是( )
| A. | W、X形成的化合物只含有离子键 | B. | 原子半径:Y>Z>W | ||
| C. | 还原性:W2->Y2- | D. | 氧化物的水化物酸性:Y<Z |