题目内容
18.A、B、C、D、E、F均为短周期主族元素,它们的原子序数依次增大,其中A的阴离子的核外电子数与B、C、D 原子的核外内层电子数相同.B的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产D的单质,E的原子序数为D的两倍.根据以上叙述,下列说法中正确的是( )| A. | 上述六种元素的原子半径大小为A<B<C<D<F<E | |
| B. | A、B、D三种元素可形成既含极性共价键又含非极性共价键的化合物 | |
| C. | A、B、C、F原子的核外最外层电子数的总和为18 | |
| D. | 由A与B组成的化合物的沸点一定低于由A与D组成的化合物的沸点 |
分析 A的阴离子的核外电子数与B、C、D 原子的核外内层电子数相同,A应为H元素,B的一种核素在考古时常用来鉴定一些文物的年代,应为C元素,工业上采用液态空气分馏方法来生产D的单质,可知C为N元素,D为O元素,E的原子序数为D的两倍,应为S元素,则F为Cl元素,结合对应单质、化合物的性质以及元素周期律解答该题.
解答 解:由以上分析可知A为H、B为C、C为N、D为O、E为S、F为Cl元素.
A.同周期元素从左到右,原子半径逐渐减小,则应为B>C>D,故A错误;
B.A、B、D三种元素形成的H2O2中,既含极性共价键又含非极性共价键,故B正确;
C.A、B、C、F原子的核外最外层电子数的总和为1+4+5+7=17,故C错误;
D.由A与B组成的化合物为烃类物质,如含有C原子数目较多,常温下为固体,则沸点大于水等,故D错误.
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的性质推断元素为解答本题的关键,侧重分析与应用的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
9.下列说法不正确的是( )
| A. | 油脂发生皂化反应能生成甘油 | |
| B. | 丙烷和2-甲基丙烷的一氯代物均为两种 | |
| C. | 酿酒过程中,葡萄糖可通过水解反应生成酒精 | |
| D. |  ≡C-COOH是高分子化合物 ≡C-COOH是高分子化合物 的单体 的单体 |
13.下列叙述正确的是( )
| A. | 以可逆反应为原理的原电池发生反应达平衡时,该电池仍有电流产生 | |
| B. | 使用催化剂能够降低正、逆反应的活化能和△H | |
| C. | 金属发生吸氧腐蚀时,被腐蚀的速率和溶解氧的浓度无关 | |
| D. | 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中氯离子和溴离子浓度的比值不变 |
3.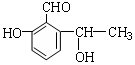 某有机物的结构简式如图,它可能发生的反应类型有( )
某有机物的结构简式如图,它可能发生的反应类型有( )
①取代 ②加成 ③消去 ④水解⑤酯化 ⑥中和 ⑦氧化 ⑧加聚.
 某有机物的结构简式如图,它可能发生的反应类型有( )
某有机物的结构简式如图,它可能发生的反应类型有( )①取代 ②加成 ③消去 ④水解⑤酯化 ⑥中和 ⑦氧化 ⑧加聚.
| A. | ①②③④⑥ | B. | ②③④⑤⑧ | C. | ③④⑤⑥⑦ | D. | ①②③⑤⑥⑦ |
1.NA代表阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,22.4LCl2与足量的铁粉反应,转移的电子数为3NA | |
| B. | 含23g钠元素的Na2O和Na2O2混合物中阴离子数目介于0.5NA和NA之间 | |
| C. | 在0℃、101kPa条件下,11.2L丁烷中含极性共价键数目为5NA | |
| D. | 5NH4NO3$\frac{\underline{\;△\;}}{\;}$4N2↑+2HNO3+9H2O中氧化产物比还原产物每多14g,转移电子数为15NA |
18.在1200℃时,天然气脱硫工艺中会发生下列反应,则△H4的正确表达式为( )
①H2S(g)+$\frac{3}{2}$O2(g)=SO2(g)+H2O(g)△H1②2H2S(g)+SO2(g)=$\frac{3}{2}$S2(g)+2H2O(g)△H2
③H2S(g)+$\frac{1}{2}$O2(g)=S(g)+H2O(g)△H3④S(g)=$\frac{1}{2}$S2(g)△H4.
①H2S(g)+$\frac{3}{2}$O2(g)=SO2(g)+H2O(g)△H1②2H2S(g)+SO2(g)=$\frac{3}{2}$S2(g)+2H2O(g)△H2
③H2S(g)+$\frac{1}{2}$O2(g)=S(g)+H2O(g)△H3④S(g)=$\frac{1}{2}$S2(g)△H4.
| A. | △H4=$\frac{1}{3}$(3△H3-△H1-△H2) | B. | △H4=$\frac{1}{3}$(△H1+△H2-3△H3) | ||
| C. | △H4=$\frac{3}{4}$(△H1+△H2-3△H3) | D. | △H4=$\frac{3}{4}$(△H1-△H2-3△H3) |
19.提纯分离下述物质时,采用的方法与制取无水乙醇的方法相同的是( )
| A. | 分离硬脂酸和甘油 | B. | 除去乙醛中少量醋酸 | ||
| C. | 分离苯酚和苯 | D. | 除去甲烷中少量乙烯 |

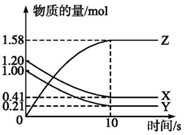 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: