题目内容
20.模型在研究物质的结构和变化有很重要的作用.如图表示乙烯(C2H4)、甲醛(HCHO)和物质甲的分子结构模型.下列叙述错误的是( )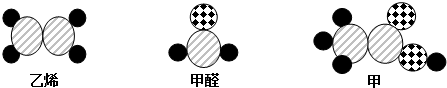
| A. | 物质甲的分子式为C2H4O2 | |
| B. | 若物质甲具有酸性,则乙烯和甲醛一定具有酸性 | |
| C. | 物质甲、乙烯和甲醛分子都具有双键 | |
| D. | 若三种物质在空气中完全燃烧,生成的产物相同 |
分析 由结构模型可知甲为乙酸,具有酸性,甲醛含有醛基,乙烯含有碳碳双键,以此解答该题.
解答 解:A.物质甲为乙酸,分子式为C2H4O2,故A正确;
B.乙烯和甲醛没有酸性,都为非电解质,故B错误;
C.乙烯含有碳碳双键,甲醛、乙酸含有C=O键,故C正确;
D.都含有C、H,燃烧产物为水和二氧化碳,故D正确.
故选B.
点评 本题考查球棍模型与比例模型以及有机物的结构和性质,注意习题中的信息分析物质的性质,把握官能团与性质的关系为解答的关键,题目难度不大.

练习册系列答案
相关题目
11.最近科学家发现了一种新分子,它具有空心的类似足球的结构,分子式为C60,下列说法正确的是( )
| A. | C60是一种新型的化合物 | |
| B. | C60和石墨都是碳的同素异形体 | |
| C. | C60中虽然没有离子键,但固体为离子晶体 | |
| D. | C60相对分子质量为720 g/mol |
8.下列化学用语或命名正确的是( )
| A. | 次氯酸的结构式:H-Cl-O | |
| B. | 含有10个中子的氧原子的符号:${\;}_{8}^{18}$O | |
| C. | S2-的结构示意图 | |
| D. | NH4Cl的电子式: |
15.通过强烈的相互作用形成金属键的微粒的是( )
| A. | 阴阳离子 | B. | 原子 | ||
| C. | 分子 | D. | 金属阳离子和自由电子 |
5.电解质有强弱之分,以下物质属于强电解质的是( )
| A. | 水 | B. | 氨水 | C. | 醋酸 | D. | 氯化钠 |
12.下列反应中,没有表现出硫酸的氧化性的是( )
| A. | Cu+H2SO4 | B. | C+H2SO4 | C. | H2S+H2SO4 | D. | NaCl+H2SO4 |
9.下列叙述不正确的是( )
| A. | CH4与C4H10互为同系物 | |
| B. | 23592U和23892U质子数相同,二者属于同一种核素 | |
| C. | 蔗糖和麦芽糖都属于双糖,且互为同分异构体 | |
| D. | 苯分子中的碳碳键是介于单键和双键之间的独特的键 |
10.下列除杂方案合理的是( )
| A. | 除去溴苯中少量的溴:加入苯萃取,分液 | |
| B. | 除去乙酸乙酯中的少量乙酸:加入饱和Na2CO3溶液,分液 | |
| C. | 除去乙烯中少量的SO2:气体通过盛有酸性高锰酸钾溶液的洗气瓶 | |
| D. | 除去MgCl2溶液中少量的FeCl3:加入稍过量氢氧化钠,过滤 |
 图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水.向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝.
图中硬质试管A中放入干燥洁净的细铜丝,烧杯中放入温水,试管B中放入甲醇,右方试管C中放入冷水.向B中不断鼓入空气,使甲醇蒸气和空气通过加热到红热程度的铜丝.