题目内容
10.下列除杂方案合理的是( )| A. | 除去溴苯中少量的溴:加入苯萃取,分液 | |
| B. | 除去乙酸乙酯中的少量乙酸:加入饱和Na2CO3溶液,分液 | |
| C. | 除去乙烯中少量的SO2:气体通过盛有酸性高锰酸钾溶液的洗气瓶 | |
| D. | 除去MgCl2溶液中少量的FeCl3:加入稍过量氢氧化钠,过滤 |
分析 A.溴、苯、溴苯混溶;
B.乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应;
C.二者都与高锰酸钾反应;
D.二者都与氢氧化钠溶液反应.
解答 解:A.溴、苯、溴苯混溶,不能用于除杂,应用氢氧化钠溶液,故A错误;
B.乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应,可用分液的方法除杂,故B正确;
C.二者都与高锰酸钾反应,应用氢氧化钠溶液除杂,故C错误;
D.二者都与氢氧化钠溶液反应,可用碳酸镁或氢氧化镁除杂,故D错误.
故选B.
点评 本题考查除杂,为高频考点,明确物质的性质及发生的化学反应是解答的关键,注意除杂的原则不能引入新杂质,侧重物质性质的考查,题目难度不大.

练习册系列答案
相关题目
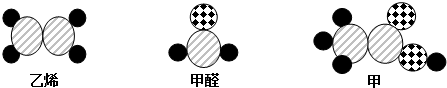
20.模型在研究物质的结构和变化有很重要的作用.如图表示乙烯(C2H4)、甲醛(HCHO)和物质甲的分子结构模型.下列叙述错误的是( )

| A. | 物质甲的分子式为C2H4O2 | |
| B. | 若物质甲具有酸性,则乙烯和甲醛一定具有酸性 | |
| C. | 物质甲、乙烯和甲醛分子都具有双键 | |
| D. | 若三种物质在空气中完全燃烧,生成的产物相同 |
1.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 在常温、常压下,11.2升N2含有的分子数为0.5 NA | |
| B. | 标准状况下,22.4LH2和O2的混合气体所含的分子数为NA | |
| C. | 标准状况下,18g H2O的体积是22.4L | |
| D. | 1mol任何物质的体积在标准状况下都约是22.4L |
5.化学与生产、生活、社会等密切相关.下列叙述正确的是( )
| A. | 碘遇淀粉变蓝,故在厨房里可用米汤检验加碘食盐中的碘 | |
| B. | 煤的气化、液化、干馏以及石油的分馏、裂化、裂解均属化学变化 | |
| C. | 明矾和氯气常用作自来水的净化与消毒,其作用原理相同 | |
| D. | 维生素C有还原性,故苹果汁中加入维生素C可防止变黄 |
19.常温下0.1mol•L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
| A. | 将溶液稀释到原体积的2倍 | B. | 加入适量的醋酸钠固体 | ||
| C. | 加入等体积0.2 mol•L-1盐酸 | D. | 加少量冰醋酸 |