题目内容
9.下列叙述不正确的是( )| A. | CH4与C4H10互为同系物 | |
| B. | 23592U和23892U质子数相同,二者属于同一种核素 | |
| C. | 蔗糖和麦芽糖都属于双糖,且互为同分异构体 | |
| D. | 苯分子中的碳碳键是介于单键和双键之间的独特的键 |
分析 A.具有同一通式、组成上相差一个或多个CH2原子团、在结构与性质上相似的化合物为同系物;
B.核素是含有一定数目的质子和中子数的原子;
C.同分异构体是分子式相同结构式不同的化合物;
D.苯分子中的碳碳键是介于单键和双键之间的独特的化学键.
解答 解:A.甲烷(CH4)和丁烷(C4H10)满足通式为CnH2n+2,结构相似,分子组成上相差2个CH2原子团,属于同系物,故A正确;
B.元素符号左下角Z代表质子数、左上角A代表质量数,质量数=质子数+中子数;23592U和23892U质子数相同,中子数分别为143、146,核素是含有一定数目的质子和中子数的原子,属于不同核素,故B错误;
C.蔗糖和麦芽糖是双糖,分子式都可用C12H22O11表示,它们互为同分异构体,故C正确;
D.苯分子中的碳原子采取sp2杂化,6个碳原子中未参与杂化的2p轨道以“肩并肩”形式形成一个大π键,苯分子呈平面正六边形,6个碳碳键完全相同,是介于单键和双键之间的一种特殊类型的键,故D正确;
故选B.
点评 本题考查同系物、核素、同分异构体、苯分子结构等,题目难度不大,侧重对基础知识的巩固,注意概念的内涵和外延.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
19.过氧化钾与水的反应类似于过氧化钠与水的反应,其化学方程式为:2K2O2+2H2O=4KOH+O2↑当0.5mol K218O2与足量H2O完全反应后,下表对生成物O2的叙述中错误的是( )
| K218O2的质量 | O2的叙述 | |
| A | 57g | O2的质量为9g |
| B | 57g | 生成标准情况下O2的体积为5.6L |
| C | 114g | O2的摩尔质量是32g•mol-1 |
| D | 57g | 生成0.25molO2 |
| A. | A | B. | B | C. | C | D. | D |
20.模型在研究物质的结构和变化有很重要的作用.如图表示乙烯(C2H4)、甲醛(HCHO)和物质甲的分子结构模型.下列叙述错误的是( )
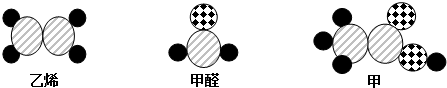

| A. | 物质甲的分子式为C2H4O2 | |
| B. | 若物质甲具有酸性,则乙烯和甲醛一定具有酸性 | |
| C. | 物质甲、乙烯和甲醛分子都具有双键 | |
| D. | 若三种物质在空气中完全燃烧,生成的产物相同 |
17.下列离子方程式书写正确的是( )
| A. | 氨水跟盐酸反应:OH-+H+→H2O | |
| B. | 铁与硝酸银溶液反应:Fe+Ag+→Fe2++Ag | |
| C. | 氢氧化铜与稀硫酸反应:Cu(OH)2+2H+→Cu2++2H2O | |
| D. | 氢氧化钡跟稀硫酸反应:Ba2++OH-+H++SO42-→BaSO4↓+H2O |
14.依据反应原理回答下列问题:
Ⅰ.请你利用原电池原理,设计实验,比较铜和铁的金属活动性.
实验用品:铁片、铜片、导线、金属夹、小灯泡、硫酸亚铁溶液、硫酸铜溶液、500mL烧杯.
画出实验装置简图,并标出正负极、电子流动方向.
Ⅱ.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
(1)过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;氯化铁\;}}{\;}$2H2O+O2↑.
(2)实验①的目的是研究温度对H2O2分解速率的影响.
实验中滴加FeCl3溶液的目的是加快H2O2分解速率,使实验现象易于观察.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/LFeCl3溶液,观察产生气泡的速率(用实验中所提供的几种试剂).
(4)某同学在50mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图2所示,则A、B、C三点所表示的瞬时反应速率最慢的是C.
(5)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图3甲、乙所示的实验.请回答相关问题:
①定性分析:如图甲可通过观察溶液中气泡产生的速率,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是排除氯离子的干扰.
②定量分析:用图3乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是收集40mL气体所需的时间.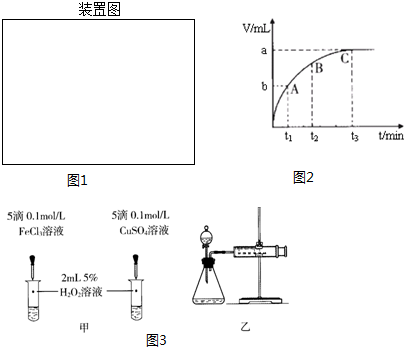
Ⅰ.请你利用原电池原理,设计实验,比较铜和铁的金属活动性.
实验用品:铁片、铜片、导线、金属夹、小灯泡、硫酸亚铁溶液、硫酸铜溶液、500mL烧杯.
画出实验装置简图,并标出正负极、电子流动方向.
Ⅱ.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入3mL 5% H2O2溶液,各滴入2滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. | 试管A中不再产生气泡; 试管B中产生的气泡量增大. |
| ② | 另取两支试管分别加入3mL 5% H2O2溶液和3mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生. |
(2)实验①的目的是研究温度对H2O2分解速率的影响.
实验中滴加FeCl3溶液的目的是加快H2O2分解速率,使实验现象易于观察.
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/LFeCl3溶液,观察产生气泡的速率(用实验中所提供的几种试剂).
(4)某同学在50mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图2所示,则A、B、C三点所表示的瞬时反应速率最慢的是C.
(5)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图3甲、乙所示的实验.请回答相关问题:
①定性分析:如图甲可通过观察溶液中气泡产生的速率,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是排除氯离子的干扰.
②定量分析:用图3乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是收集40mL气体所需的时间.

1.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 在常温、常压下,11.2升N2含有的分子数为0.5 NA | |
| B. | 标准状况下,22.4LH2和O2的混合气体所含的分子数为NA | |
| C. | 标准状况下,18g H2O的体积是22.4L | |
| D. | 1mol任何物质的体积在标准状况下都约是22.4L |
19.常温下0.1mol•L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
| A. | 将溶液稀释到原体积的2倍 | B. | 加入适量的醋酸钠固体 | ||
| C. | 加入等体积0.2 mol•L-1盐酸 | D. | 加少量冰醋酸 |