题目内容
4.下列对有关元素的叙述能说明该元素一定是主族元素的是( )| A. | 原子最外层电子数为2的元素 | |
| B. | 原子序数为48的元素 | |
| C. | 原子核外L层比M层多一个电子的元素 | |
| D. | 原子核外M层有8个电子的元素 |
分析 A.原子最外层电子数为2的元素可能处于ⅡA族、可能为过渡元素、可能为He;
B.原子序数为48的元素为Cd元素;
C.原子核外L层比M层多一个电子的元素为Cl;
D.原子核外M层有8个电子的元素,可能为Ar或其它元素.
解答 解:A.原子最外层电子数为2的元素可能处于ⅡA族、可能为过渡元素、可能为He,不一定是主族元素,故A错误;
B.原子序数为48的元素为Cd元素,为过渡金属元素,故B错误;
C.原子核外L层比M层多一个电子的元素为Cl,为ⅦA元素,故C正确;
D.原子核外M层有8个电子的元素,可能为Ar或其它元素,不能确定其它元素,但Ar不是主族,故D错误.
故选C.
点评 本题考查元素周期表结构及应用,为高频考点,根据外围电子排布确定元素在周期表中族问题,注意外围电子与最外层电子不同,难度不大.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
14.下列分子中所有原子均满足最外层8电子结构的是( )
| A. | LiCl | B. | NCl3 | C. | PCl5 | D. | BF3 |
12.X、Y是元素周期表ⅦA族中的两种元素,X的非金属性比Y的强.则下列叙述中,正确的是( )
| A. | X原子的电子层数比Y原子的电子层数多 | |
| B. | X的单质一定能将Y从NaY的水溶液中置换出来 | |
| C. | X的单质比Y的单质更容易与氢气反应 | |
| D. | X的氢化物水溶液的酸性一定比Y的氢化物水溶液的酸性强 |
9.某同学探究溶液的酸碱性对FeCl3水解平衡的影响,实验方案如下:
配制50mL0.001mol/L FeCl3溶液、50mL对照组溶液x,向两种溶液中分别滴加1滴1mol/L HCl溶液、1滴1mol/L NaOH 溶液,测得溶液pH随时间变化的曲线如图所示.下列说法不正确的是( )
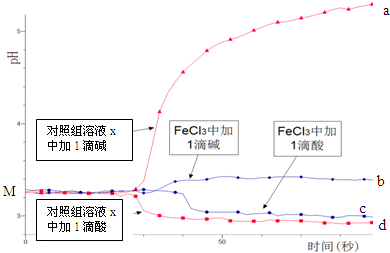
配制50mL0.001mol/L FeCl3溶液、50mL对照组溶液x,向两种溶液中分别滴加1滴1mol/L HCl溶液、1滴1mol/L NaOH 溶液,测得溶液pH随时间变化的曲线如图所示.下列说法不正确的是( )

| A. | 依据M点对应的pH,说明Fe3+发生了水解反应 | |
| B. | 对照组溶液x的组成可能是0.003 mol/L KCl | |
| C. | 依据曲线c和d说明Fe3+水解平衡发生了移动 | |
| D. | 通过仪器检测体系浑浊度的变化,可表征水解平衡移动的方向 |
16.铜是一种紫红色金属,被称作“电器工业的主角”铜主要是黄铜矿炼制,焙烧时发生反应2CuFeS2+O2$\frac{\underline{\;高温\;}}{\;}$Cu2S+2FeS+SO2,其简单流程如图所示,下列说法正确的是( )
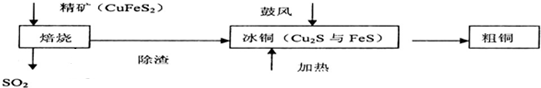

| A. | 焙烧时硫元素全部转化为二氧化硫 | B. | 在焙烧时氧化剂只有氧气 | ||
| C. | 粗铜精炼时用粗铜做阴极 | D. | Cu2S可用于火法炼制铜 |
13.下列说法正确的是( )
| A. | 各元素的最高正化合价跟族的序数相等 | |
| B. | 所有元素都有正化合价和负化合价,它们的绝对值之和等于8 | |
| C. | 非金属元素的负化合价,等于原子最外层达到8个电子稳定结构所需得到的电子数 | |
| D. | 各元素原子的最外层电子数跟族序数相等 |