题目内容
(1)氯气通入水中的反应方程式为: .
(2)铝与氢氧化钠溶液反应的离子方程式为: .
(3)玻璃是重要的硅酸盐产品.生产玻璃时,石灰石与石英反应的化学方程式为 .
(4)氟氯代烷是一种能破坏臭氧层的物质.在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:①Cl+O3→ClO+O2 ②O3
O+O2 ③ClO+O→Cl+O2
上列反应的总反应式是 ,
(5)对汽车加装尾气催化净化装置,可以使其中的NO、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为 .
(2)铝与氢氧化钠溶液反应的离子方程式为:
(3)玻璃是重要的硅酸盐产品.生产玻璃时,石灰石与石英反应的化学方程式为
(4)氟氯代烷是一种能破坏臭氧层的物质.在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:①Cl+O3→ClO+O2 ②O3
| 光照 |
上列反应的总反应式是
(5)对汽车加装尾气催化净化装置,可以使其中的NO、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为
考点:氯气的化学性质,硅和二氧化硅,铝的化学性质,卤代烃简介
专题:元素及其化合物
分析:(1)氯气与水反应生成氯化氢和次氯酸;
(2)金属铝与氢氧化钠溶液反应生成了偏铝酸钠和氢气,据此写出反应的离子方程式;
(3)石灰石与石英反应生成硅酸钙和二氧化碳;
(4)将方程式①②③相加得出氧气和臭氧的关系式;
(5)根据反应物与生成物来书写化学方程式;
(2)金属铝与氢氧化钠溶液反应生成了偏铝酸钠和氢气,据此写出反应的离子方程式;
(3)石灰石与石英反应生成硅酸钙和二氧化碳;
(4)将方程式①②③相加得出氧气和臭氧的关系式;
(5)根据反应物与生成物来书写化学方程式;
解答:
解:(1)氯气通入水中反应生成氯化氢和次氯酸,反应的离子方程式为:Cl2+H2O=HCl+HClO;
故答案为:Cl2+H2O=HCl+HClO;
(2)铝与氢氧化钠溶液反应,反应生成偏铝酸钠和氢气,该离子反应为:2Al+2H2O+2OH-═2AlO2-+3H2↑,
故答案为:2Al+2H2O+2OH-═2AlO2-+3H2↑;
(3)石灰石与石英反应生成硅酸钙和二氧化碳,反应化学方程式为:CaCO3+SiO2
CaSiO3+CO2↑;
故答案为:CaCO3+SiO2
CaSiO3+CO2↑;
(4)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3
3O2;
故答案为:2O3
3O2;
(5)由NO、CO相互反应转换成无毒的气体,即生成氮气和二氧化碳,该反应的化学反应方程式为2NO+2CO
N2+2CO2;
故答案为:2NO+2CO
N2+2CO2.
故答案为:Cl2+H2O=HCl+HClO;
(2)铝与氢氧化钠溶液反应,反应生成偏铝酸钠和氢气,该离子反应为:2Al+2H2O+2OH-═2AlO2-+3H2↑,
故答案为:2Al+2H2O+2OH-═2AlO2-+3H2↑;
(3)石灰石与石英反应生成硅酸钙和二氧化碳,反应化学方程式为:CaCO3+SiO2
| ||
故答案为:CaCO3+SiO2
| ||
(4)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3
| ||
故答案为:2O3
| ||
(5)由NO、CO相互反应转换成无毒的气体,即生成氮气和二氧化碳,该反应的化学反应方程式为2NO+2CO
| ||
故答案为:2NO+2CO
| ||
点评:本题考查了化学方程式、离子方程式的书写,题目较简单,侧重对学生能力的培养和训练,注意掌握化学方程式和离子方程式的书写方法.

练习册系列答案
相关题目
下列关于稀有气体的叙述不正确的是( )
| A、各原子轨道电子均已填满 |
| B、其原子与同周期ⅠA、ⅡA族阳离子具有相同的核外电子排布 |
| C、化学性质非常不活泼 |
| D、同周期中第一电离能最大 |
下列微粒中不能破坏水的电离平衡的是( )
| A、Na HSO4 |
| B、Al3+ |
| C、CO32- |
| D、K+ |
下列性质不是由氢键引起的( )
| A、水的熔点比硫化氢高 |
| B、H-F的键能很大 |
| C、乙醇与水能以任意比例混溶 |
| D、冰的密度比水小 |
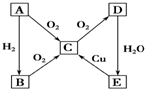 在通常状况下,A为固态单质.根据图转化关系,回答:
在通常状况下,A为固态单质.根据图转化关系,回答: