题目内容
某学生欲用浓12mol?L-1盐酸和蒸馏水配制500mL物质的量浓度为0.600mol/L的稀盐酸.求该学生需要量取多少 mL上述浓盐酸进行配制?
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:溶液稀释过程中溶质的物质的量不变,即c(浓)×V(浓)=c(稀)×V(稀),据此列式计算出配制500mL物质的量浓度为0.600mol/L的稀盐酸,需要浓盐酸的体积.
解答:
解:浓溶液在稀释过程中,溶质的物质的量不变,即:c(浓)×V(浓)=c(稀)×V(稀),
V(浓)=
=
=0.025 L=25 mL,
答:配制该稀溶液需要浓盐酸的体积为25mL.
V(浓)=
| c(稀)V(稀) |
| c(浓) |
| 0.600mol/L×0.5L |
| 12mol/L |
答:配制该稀溶液需要浓盐酸的体积为25mL.
点评:本题考查了溶液稀释的计算,题目难度不大,注意掌握物质的量浓度的概念及计算方法,明确溶液稀释过程中c(浓)×V(浓)=c(稀)×V(稀)为解答本题的关键.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
下列解释实验现象的反应方程式正确的是( )
| A、向Na2CO3溶液中滴入酚酞试液,溶液变红CO32-+2H2O?H2CO3+2OH- |
| B、向AgC1悬浊液中滴加Na2S溶液,白色沉淀变成黑色2AgC1+S2-=Ag2S↓+2C1- |
| C、铜器在潮湿的环境中表面生成一层“铜绿”:Cu+O2+CO2=CuCO3 |
| D、向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
下列有机物命名正确的是( )
A、1,3,4-三甲苯 |
B、α-氨基苯丙酸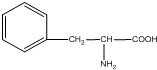 |
| C、2-甲基丙烯 (CH3)2C=CH2 |
| D、2,2-二甲基-3-丁醇 (CH3)3C-CHOH-CH3 |
下列关于化学反应的速率和限度的说法正确的是( )
| A、化学反应速率通常只能用反应物浓度的减少量表示 |
| B、化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| C、影响化学反应速率的条件并不只是温度和催化剂 |
| D、催化剂都能加快化学反应速率,并提高原料利用率或转化率 |
下列说法正确的是( )
| A、pH=2和pH=1的硝酸中c(H+)之比为10:1 | ||
| B、一元酸与一元碱恰好完全反应后的溶液中一定存在c(H+)=c(OH-) | ||
C、KAl(SO4)2溶液中离子浓度的大小顺序为c(SO
| ||
| D、常温下,将pH均为12的氨水和NaOH溶液分别加水稀释100倍后,NaOH溶液的pH较大 |
 (1)如图为干冰的晶胞结构,观察图形,确定在干冰中每个CO2分子周围有
(1)如图为干冰的晶胞结构,观察图形,确定在干冰中每个CO2分子周围有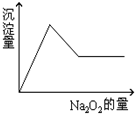 有一透明溶液,可能含有Al3+、Fe3+、K+、Mg2+和Cu2+等离子中的一种或几种.现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀.如加入Na2O2的量与生成白色沉淀的量之间的关系用图来表示.
有一透明溶液,可能含有Al3+、Fe3+、K+、Mg2+和Cu2+等离子中的一种或几种.现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀.如加入Na2O2的量与生成白色沉淀的量之间的关系用图来表示.