题目内容
13.目前人工合成高效青蒿素主要采用青蒿酸为原料半合成法.青蒿酸的结构简式如图A所示.下列有关说法正确的是( )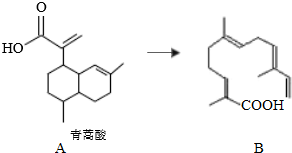
| A. | 青蒿酸的分子式为C15H20O2 | |
| B. | 1mol青蒿酸最多可与3molH2加成 | |
| C. | 青蒿酸与B互为同分异构体 | |
| D. | 苯环上连有-CHO和-OH、分子中有6种不同化学环境氢的青蒿酸的同分异构体只有2种 |
分析 A.由结构简式可知青蒿素的分子式为C15H22O2;
B.1mol青蒿酸中含有2mol碳碳双键,最多可与2molH2加成;
C.青蒿酸与B的分子式均为C15H22O2,但结构不同,故互为同分异构体;
D.苯环上连有-CHO和-OH、分子中有6种不同化学环境氢的青蒿酸的同分异构体,苯环上醛基与羟基处在对位,同分异构体有 3种.
3种.
解答 解:A.由结构简式可知青蒿素的分子式为C15H22O2,故A错误;
B.1mol青蒿酸中含有2mol碳碳双键,最多可与2molH2加成,故B错误;
C.青蒿酸与B的分子式均为C15H22O2,但结构不同,故互为同分异构体,故C正确;
D.苯环上连有-CHO和-OH、分子中有6种不同化学环境氢的青蒿酸的同分异构体,苯环上醛基与羟基处在对位,同分异构体有 3种,故D错误.
3种,故D错误.
故选C.
点评 本题考查有机物的结构性质,为高频考点,把握结构中的环状及酯的性质为解答的关键,侧重分析能力和知识迁移应用能力的考查,注意有机物分子式由结构中化学键分析,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.原子序数依次增大的短周期元素a、b、c、d,它们的最外层电子数分别为6、7、1、3.a、b、c、d形成的简单离子与氖原子电子层结构相同.下列叙述错误的是( )
| A. | 元素的非金属性顺序为a>b | |
| B. | a和c形成的离子化合物中可能含有共价键 | |
| C. | d的最高价氧化物对应的水化物可溶于c的最高价氧化物对应水化物的水溶液 | |
| D. | 五种元素离子半径最小的是d |
4.下列说法正确的是( )
| A. | 相同条件下,测得Na2CO3溶液的pH大于相同物质的量浓度的Na2SO3溶液,说明非金属性:C<S | |
| B. | 绝热容器中,向50 mL 1 mol•L-1的盐酸中加入烧碱,水的KW不变 | |
| C. | 相同温度时,BaSO4分别在相同物质的量浓度的Na2SO4溶液和Al2(SO4)3溶液中的溶解度相同 | |
| D. | 有HX和HY两种弱酸且酸性HX>HY,则物质的量浓度相同的NaX和NaY两溶液等体积混合的溶液中有 c(X-)>c(Y-)>c(OH-)>c(H+) |
1.四种短周期元素X、Y、Z、W的原子序数依次增大,X、W原子序数之和等于Y、Z原子序数之和.X、W两元素位于同一主族,Y元素是其所在周期中原子半径最大的元素(惰性气体元素除外),Z的单质是银白色固体,易导电,常温下不易溶于浓硫酸.下列有关推断错误的是( )
| A. | X的氢化物的沸点高于同族其他元素氢化物的沸点 | |
| B. | 阴离子还原性:X>W;阳离子氧化性:Z>Y | |
| C. | X与Y两种元素可形成含有共价键的离子化合物 | |
| D. | Z与W两种元素形成的化合物在水溶液中不能存在 |
8.纳米CdSe(硒化镉)可用作光学材料.在一定条件下,由Na2SO3和Se反应生成Na2SeSO3(硒代硫酸钠);再由CdCl2形成的配合物与Na2SeSO3反应制得CdSe纳米颗粒.流程图如下:
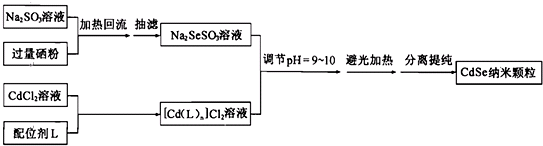
已知:①纳米颗粒通常指平均粒径为1~100nm的粒子
②CdSe纳米颗粒的大小影响会其发光性质.在一定配位剂浓度下,避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,结果如图1所示;某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图2所示:

则下列说法中正确的是( )

已知:①纳米颗粒通常指平均粒径为1~100nm的粒子
②CdSe纳米颗粒的大小影响会其发光性质.在一定配位剂浓度下,避光加热步骤中反应时间和温度对纳米颗粒平均粒径的影响,结果如图1所示;某温度下配位剂浓度对纳米颗粒平均粒径的影响,如图2所示:

则下列说法中正确的是( )
| A. | 在分离提纯CdSe时一般向溶液中加入丙酮,以增强溶剂极性,有利于CeSe的沉淀,提高收率 | |
| B. | 一般可用NaOH调节Na2SeSO3溶液的pH值,在此过程中会有HSe-和HSO3-生成 | |
| C. | 该纳米颗粒不能使用常压过滤或者减压过滤分离,因为其易在滤纸表面形成一层致密而厚实的膜,阻碍溶剂的通过 | |
| D. | 改变反应温度和反应时间,可以得到不同发光性质的CdSe纳米颗粒;且若要在60℃得到3.0 nm的CdSe纳米颗粒,可尝试降低配位剂浓度的方法 |
18.乙醇是一种优质的液体燃料,二甲醚与合成气制乙醇是目前合成乙醇的一种新途径,总反应为:CH3OCH3(g)+CO(g)+2H2(g)?CH3OH(g)+C2H5OH(g).向反应系统中同时通入二甲醚、一氧化碳和氢气,先生成中间产物乙酸甲酯后,继而生成乙醇.发生的主要化学反应有:
回答下列问题:二甲醚碳基化反应的△H<0 (填“>”“<”“=”).
| 反应过程 | 化学方程式 | 不同温度下的K | ||
| 273.15K | 1000K | |||
| Ⅰ | 二甲醚羰基化反应 | CH3OCH3(g)+CO(g)?CH3COOCH3(g) | 1016.25 | 101.58 |
| Ⅱ | 乙酸甲酯加氢反应 | CH3COOCH3(g)+2H2(g)?CH3OH(g)+C2H5OH(g) | 103.97 | 10-0.35 |
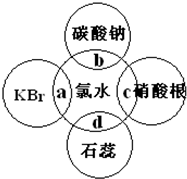 氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量).
氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量).